
| A. | Na+的电子排布图: | B. | Na+的结构示意图: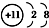 | ||
| C. | Na的电子排布式:1s22s22p63s1 | D. | Na的简化电子排布式:[Ne]3s1 |
分析 A.同一轨道内的2个电子自旋方向应该相反;
B.Na+核外电子数为10,有2个电子层,各层电子数为2、8;
C.Na原子核外电子数为11;
D.钠原子的内层电子排布为1s22s22p6,应是Ne的排布式.
解答 解:A.同一轨道内的2个电子自旋方向应该相反,钠原子失去3s的1个电子形成钠离子,钠离子核外有10个电子,Na+的电子排布图: ,故A错误;
,故A错误;
B.Na+核外电子数为10,有2个电子层,各层电子数为2、8,结构示意图为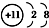 ,故B正确;
,故B正确;
C.Na原子核外电子数为11,则钠原子的核外电子排布式为1s22s22p63s1,故C正确;
D.钠原子的核外电子排布式为1s22s22p63s1,内层电子排布为1s22s22p6,Na原子的简化电子排布式:[Ne]3s1,故D正确;
故选A.
点评 本题考查常用化学用语的书写,难度中等,注意理解掌握核外电子排布规律.


科目:高中化学 来源: 题型:选择题
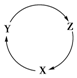 下列各组物质中,满足如图物质一步转化关系的选项是( )
下列各组物质中,满足如图物质一步转化关系的选项是( )| 选项 | X | Y | Z |
| A | Na | NaOH | NaHCO3 |
| B | S | SO2 | SO3 |
| C | C | CO | CO2 |
| D | Si | SiO2 | H2SiO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
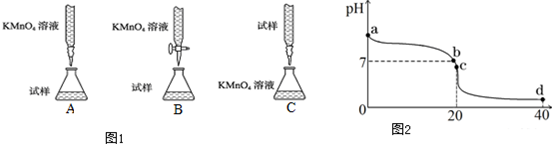
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 滴定次数 | 标准溶液的体积/mL | 待测盐酸溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 1.05 | 21.10 | 15.00 |
| 2 | 2.00 | 21.95 | 15.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com