
下列说法正确的是( )
A.HCl溶液中无OH-
B.NaOH溶液中无H+
C.KCl溶液中既无H+也无OH-
D.常温下,任何物质的水溶液中都有H+和OH-,且KW=1×10-14 mol2·L-2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
中央电视台曾报道纪联华超市在售的某品牌鸡蛋为“橡皮弹”, 煮熟后蛋黄韧性胜过乒乓球,但经检测为真鸡蛋。专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚所致。其结构简式如右图所示:下列说法不正确的是
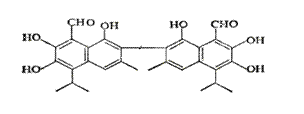
A、该化合物的分子式为:C30H30O8
B、1mol棉酚最多可与10mol H2加成,与6molNaOH反应
C、在一定条件下,可与乙酸反应生成酯类物质
D、该物质可以使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是
A.含金属元素的离子一定是阳离子
B.应用蒸馏的方法,可以分离沸点相差较大的液体混合物
C.氯水和过氧化钠都具有漂白作用,其漂白原理相似
D.高炉炼铁时,还原铁矿石的还原剂为一氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
某工业残渣主要成分为Fe2O3(含有少量FeO、Cu、Mg等杂质)某课外兴趣小组利用该残渣制取Fe2O3粉末的实验流程如下:(说明:流程中向黄色溶液中加入MgO的目的是调节溶液的酸碱性,使Fe3+ 生成沉淀而Mg2+不沉淀)
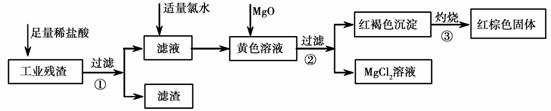
请回答下列问题:
(1)加入足量稀盐酸后,发生化学反应的类型有_____________(填写代号)。
A.置换反应 B.化合反应 C.分解反应 D.复分解反应 E.氧化还原反应
(2)加入适量氯水的作用是 ;
(3)写出灼烧红褐色沉淀时发生反应的化学方程式 。实验室灼烧红褐色沉淀可选用的装置是__________(填序号)。
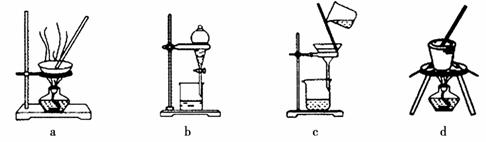
(4)若向黄色溶液中加入过滤①后的滤渣发生反应的离子方程式为 。
(5)检验黄色溶液中Fe3+是否完全沉淀的方法是:取过滤②后的少量滤液于试管中, 。(请补充完整实验操作、现象、结论)
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为10 mL一定物质的量浓度的HCl溶液用一定物质的量浓度的NaOH溶液滴定的图示。请根据图示计算:
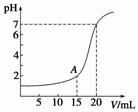
(1)氢氧化钠溶液物质的量浓度是多少?
(2)A点时溶液的pH是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C是所学过的三种单质,A、B、C及其他物质之间的反应关系如图所示,其中B、
D、E、F的水溶液呈酸性。若D+C→E+F且常温下只有B为气态,则A、B、C分别为 ( )
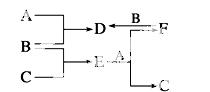
A.Fe、Cl2、Cu B.Fe、Cl2、H2
C.Cu、Cl2、Fe D.Fe、Cl2、Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol/L的硫酸,其他试剂任选。
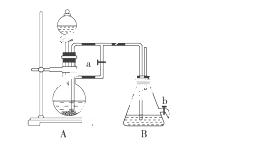
填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是________,A中反应的离子方程式是__________________________________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。
(3)简述生成Fe(OH)2的操作过程:________________________________________________。
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为________________________________________________________________________。
(5)下图中________能较长时间看到Fe(OH)2白色沉淀。
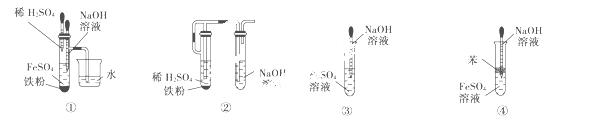
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学探究SO2有关性质。
(1)将SO2通入BaCl2溶液中,将所得溶液分成2份,在第一份中加入NaOH溶液,在第二份中滴入FeCl3溶液,两份都有白色沉淀。BaCl2溶液中通入SO2气体的现象为 ▲ 。在第二份溶液中滴入FeCl3溶液时,SO2表现 ▲ 性,反应的离子方程式为 ▲ ,生成沉淀的化学式为 ▲ 。
(2)下列不能用来吸收SO2气体的是 ▲ 。
A.KMnO4(aq) B.过量氨水 C.石灰水 D.盐酸
(3)工业废气含SO2为7%(体积分数),在同温同压下,将以上废气用废气中的O2氧化含SO3。反应后气体体积为原来气体的96.64%。则SO2的转化率为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com