
(16分)有机化工原料1,4-二苯基-1,3-丁二烯及某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
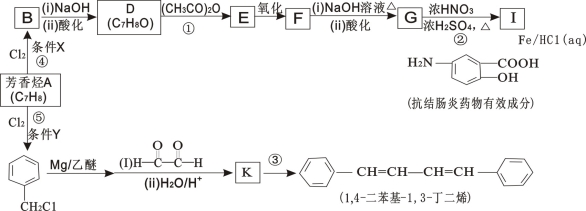
已知:
Ⅰ.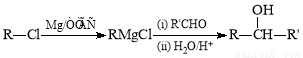 (R、R`表示烃基)
(R、R`表示烃基)
Ⅱ.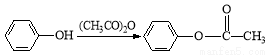
Ⅲ.
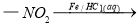

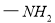
Ⅳ.

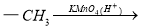

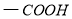
(1)抗结肠炎药物有效成分分子中的含氧官能团名称是 。
(2)D的结构简式是_______________
(3)写出F与NaOH反应的化学方程式 。
(4)下列说法正确的是________(填选项字母)。
A.④的反应条件X和⑤的反应条件Y完全相同
B.①②④⑤反应类型相同
C.G不可以发生缩聚反应
D.设计D→E和F→G两步反应的目的是防止酚羟基被氧化
(5)检验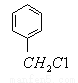 有氯原子的方法是 。
有氯原子的方法是 。
(6)③的化学方程式是 。
(7)1,4-二苯基-1,3-丁二烯有多种同分异构体,写出符合下列条件的同分异构体的结构简式: 。
a.结构中有两个苯环,无其它环状结构
b.苯环上的一硝基取代产物有两种
c.其核磁共振氢谱有3种峰,峰面积之比为3∶2∶2
科目:高中化学 来源:2014-2015河北唐山市高一下学期开学调研考试化学试卷(解析版) 题型:选择题
把0.05molNaOH固体分别加入到100ml下列溶液中,溶液导电性基本不变的是
A.自来水 B.0.5mol/L盐酸
C.0.5mol/L醋酸 D.0.5mol/L氨水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市高三联考一化学试卷(解析版) 题型:填空题
(14分)元素X、Y、Z、W、M、N原子序数依次增大,X与M、W与N分别同主族,且元素X、Y、Z、W分属两个短周期,它们四者原子序数之和为22,最外层电子数之和为16,在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,请回答下列问题:
(1)Y元素在周期表中的位置是__________________________,X、Y、Z、W、M的原子半径由大到小的顺序为:_______________(用元素符号表示)。
(2)写出Y2X2的电子式____________;Z2X4结构式 _______________。
(3)X、Z、W形成的化合物,水溶液一定显酸性的盐是______________,其原因是_____________(用离子方程式表示),该物质所含化学键的类型是_____________。
(4)均含X、W、M、N四种元素的两种化合物相互反应有刺激性气味气体放出,反应的离子方程式为_______________。
(5)火箭发动机曾经利用Z2X4作燃料X2W2作助燃剂,产物环保无污染,写出二者反应的方程式___________________。
(6)写出N W2通入硝酸钡溶液中的离子方程式 ______________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省宜宾市高三第二次诊断测试化学试卷(解析版) 题型:填空题
(15分)回收利用印刷电路板上的铜制备铜的化合物,实现资源的再利用。
(1)回收利用印刷电路板上的铜制备CuCl2。
实验室模拟回收过程如下:

已知部分物质开始沉淀和沉淀完全时的pH如下表:
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Cu(OH)2 | 4.4 | 8.0 |
请回答下列问题:
①步骤III的操作名称是 。
②下列试剂中,可以作为试剂a的是 。
A.HNO3溶液 B.Fe2(SO4)3溶液 C.FeCl3溶液
③若不加试剂b,直接加入试剂c调节溶液pH,是否可行? (填“是”或“否”),理由是 。
(2)用H2O2和硫酸共同浸泡印刷电路板制备硫酸铜。
已知:2H2O2(l)=2H2O (l) +O2(g) △H1=-196kJ/mol
H2O(l)=H2(g) +1/2O2(g) △H2=+286kJ/mol
Cu(s) +H2SO4(aq)=CuSO4(aq) +H2(g) △H3=+64kJ/mol
则Cu(s) +H2O2(l) +H2SO4(aq) =CuSO4(aq) +2H2O(l) △H = 。
(3)将反应Cu+H2O2+H2SO4=CuSO4+2H2O设计成原电池,其正极电极反应式是 。
(4)若用硝酸和硫酸共同浸泡印刷电路板制备硫酸铜,假设印刷电路板中其他成分不与酸反应,欲制取3mol纯净的硫酸铜,需要0.5 mol/L的硝酸溶液的体积是 L。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省宜宾市高三第二次诊断测试化学试卷(解析版) 题型:选择题
下列有关(NH4)2Fe(SO4)2溶液的叙述正确的是
A.该溶液中,Na+、H+、Cl-、NO3-可以大量共存
B.和新制氯水反应的离子方程式:Fe2++Cl2=Fe3++2Cl-
C.加入NaOH溶液至Fe2+刚好沉淀完全的离子方程式: Fe2++2OH-=Fe(OH)2↓
D.离子浓度关系:c(SO42-) = c(NH4+ )>c(Fe2+ )>c(H+ )>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三二诊理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.1 mol[Zn(NH3)4]Cl2中含有σ键的数目为16 NA
B.电解精炼粗铜时,每转移NA电子,阳极上溶解的铜原子数必为0.5 NA
C.3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1NA
D.60 g石英晶体中含有的Si—O键数目为2NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三“二诊”考试化学试卷(解析版) 题型:实验题
(15分)某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如下图所示(夹持仪器已略去)。
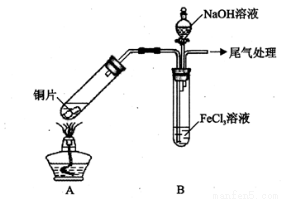
(1)实验前,应先检查装置的 ;实验中产生的尾气应通人 溶液。
(2)实验过程中需要配制100mL1mol/L FeCl3溶液(未用浓盐酸酸化),所需要的玻璃仪器有:烧杯、量筒、玻璃棒、 。
(3)该小组同学向5mL lmol/L FeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是 。
(4)该小组同学在(3)中实验时,发现溶液变为浅绿色需要较长时间,在此期间同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象,最终溶液呈浅绿色。
【查阅资料】Fe(HSO3)2+离子在溶液中呈红棕色且具有较强的还原性,能被Fe3+氧化为SO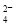 。
。
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是 。
(5)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了如下实验:

向步骤①和步骤②所得溶液中加入某种试剂,溶液立即出现蓝色沉淀,则该试剂中含有溶质的化学式是 。
(6)综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ. 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
原子序数依次增大的X、Y、Z、M、W为五种短周期元素。已知Y与Z、M与W分别同周期,X与M同主族;X、Z、M的质子数之和等于Y、W的质子数之和;X与Z、M与Z都可以分别形成A2B、A2B2型的化合物;X与Y形成的气态化合物在标准状况下的密度为0.76g·L-1;Y、M、W的最高价氧化物的水化物。两两间都能发生反应。下列说法不正确的是
A.由X、M与Z形成的化合物X2Z2和M2Z2中所含的化学键类型相同
B.含有W阳离子的某种盐,可用作净水剂
C.M的单质可保存于煤油中
D.由X、Y、Z 种元素形成的某种化合物的水溶液,可能呈碱性或酸性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东肥城市高三一模理综化学试卷(解析版) 题型:选择题
下列说法正确的是

A.蔗糖、淀粉、油脂及其水解产物均为非电解质
B.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
C.用新制Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖
D.分子所有碳原子一定不能共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com