
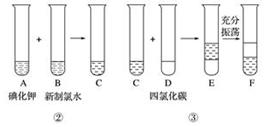
分析 (1)分离固体与液体混合物用过滤;碘在有机溶剂中溶解度远大于水,用萃取法从碘水中提取碘;氯水中氯气与碘离子反应生成单质碘和氯离子,依据反应中化合价是否有变化判断反应类型;
(2)依据四氯化碳是无色的、密度大于水的液体,是良好的有机溶剂,碘易溶于四氯化碳,结合电解质的概念判断;
(3)分离相互不溶的两种液体,应用分液法;
(4)萃取实验用到的仪器:烧杯和铁架台、玻璃棒、分液漏斗.
解答 解:(1)操作①前为悬浊液,后为溶液,可知为分离固体与液体的操作,即过滤;碘在有机溶剂中溶解度远大于水,用萃取法从碘水中提取碘,所以操作③为萃取;氯水中氯气与碘离子反应生成单质碘和氯离子,反应中-1价的碘升高为碘单质中的0价,有化合价升高,属于氧化还原反应;
故答案为:过滤;萃取 是;
(2)四氯化碳是无色的、密度大于水的液体,是良好的有机溶剂,碘易溶于四氯化碳,所以F中现象为:溶液分层,下层液体的颜色为紫红色,上层液体中溶质的主要成分为氯化钾(KCl),四氯化碳不溶于水,且不能电离产生自由移动的离子而导电,属于非电解质;
故答案为:无;大;不是; 紫红; 氯化钾(KCl);
(3)F中为相互不溶的两种液体,可用分液法分离;
故答案为:分液;
(4)萃取实验用到的仪器:烧杯和铁架台、玻璃棒、分液漏斗,
故选:C.
点评 本题以海水中提碘为载体考查了物质的分离与提纯,明确过滤、萃取、分液的原理是解题关键,侧重考查学生分析、解决问题的能量,注意对常见物质分离方法的积累.


科目:高中化学 来源: 题型:选择题
| 化学键 | Si-O | O=O | Si-Si |
| 键能kJ•mol-1 | 460 | 498.8 | X |
| A. | 423.3 | B. | 352 | C. | 920 | D. | 176 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 | |
| B. | 在气体的制备实验中,若尾气污染空气,一定要用水吸收尾气 | |
| C. | 用加热KMnO4的方法制得的氧气中常带有紫色,实验中应在试管口处放一团棉花 | |
| D. | 在点燃甲烷气体前,为防止爆炸,应先验纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=2.0×10-7mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10-4mol/L,则溶液中,由水电离产生的c(H+)=8×10-11 mol/L,此时温度高于25℃(填“高于”、“低于”或“等于”).
(1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=2.0×10-7mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10-4mol/L,则溶液中,由水电离产生的c(H+)=8×10-11 mol/L,此时温度高于25℃(填“高于”、“低于”或“等于”).查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl溶液中无OH- | |
| B. | NaOH溶液中无H+ | |
| C. | NaCl溶液中既无OH-也无H+ | |
| D. | 常温下,任何物质的水溶液中都有H+和OH-,且KW=c(H+)•c(OH-)=10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 正丁醛是一种重要的化工原料.肥西中学高二某化学兴趣小组在老师的指导下利用如图装置合成正丁醛.发生的反应如下:
正丁醛是一种重要的化工原料.肥西中学高二某化学兴趣小组在老师的指导下利用如图装置合成正丁醛.发生的反应如下:| 沸点/.c | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com