
| A.1 mol NH3与1 mol OH-所含的质子数均为10NA |
| B.标准状况下,22.4L CHCl3中含C—H键数目为NA |
| C.常温下,14 g乙烯中含碳原子数为NA |
| D.常温下,pH=13的NaOH溶液中含OH-数目为NA |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
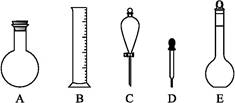
| A.50 mL 50 mL |
| B.100 mL 100 mL |
| C.100 mL 150 mL |
| D.250 mL 250 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温常压下,8.0g CH4中含有的氢原子数为2 NA |
| B.1 mol氯气跟水完全反应,转移的电子数为2 NA |
| C.1 mol Na2O2含离子数为4NA |
| D.0.1 mol/L MgCl2溶液中含氯离子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。
H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。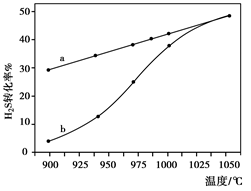

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:1 | B.2:1 | C.1:2 | D.3:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.n(盐酸)<n(稀硝酸)<n(烧碱) | B.n(烧碱)<n(盐酸)<n(稀硝酸) |
| C.n(烧碱)<n(稀硝酸)<n(盐酸) | D.n(稀硝酸)<n(烧碱)<n(盐酸) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com