


 )的一条路线如下:
)的一条路线如下:
 ;
;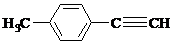 ),先发生-CHO的加成,再发生醇的消去反应,然后与溴发生加成引入两个溴原子,最后发生卤代烃在NaOH醇溶液中的消去反应生成C≡C,合成路线流程图为
),先发生-CHO的加成,再发生醇的消去反应,然后与溴发生加成引入两个溴原子,最后发生卤代烃在NaOH醇溶液中的消去反应生成C≡C,合成路线流程图为 ,据此解答.
,据此解答.
 ,
, ;
;| 84 |
| 12 |
 ),先发生-CHO的加成,再发生醇的消去反应,然后与溴发生加成引入两个溴原子,最后发生卤代烃在NaOH醇溶液中的消去反应生成C≡C,合成路线流程图为
),先发生-CHO的加成,再发生醇的消去反应,然后与溴发生加成引入两个溴原子,最后发生卤代烃在NaOH醇溶液中的消去反应生成C≡C,合成路线流程图为 ,
, ,
, ;
; ,
, ,
, ,
, 、
、 、
、 (任意2种).
(任意2种).


科目:高中化学 来源: 题型:
| 选项 | 目 的 | 分离方法 | 原 理 |
| A | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
| D | 除去丁醇中的乙醇 | 蒸馏 | 丁醇与乙醇的沸点相差较大 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,10mL 0.2mol/L NH4NO3溶液与10mL 0.1mol/L NaOH溶液混合后所得pH=9.6的溶液中:c(NO3-)>c(NH4+)>c(Na+)>c(NH3?H2O)>c(OH-)>c(H+) |
| B、0.1mol/L Na2S溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| C、常温下a mL 0.1mol/L KOH与b mL 0.1mol/L HCN两溶液混合后pH>7,则一定有a≥b |
| D、10mL 0.1mol/L NaCl溶液中离子总数为x,10mL 0.1mol/L CH3COONa溶液中离子总数为y,则x=y |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol的D37Cl分子中的中子数是2NA |
| B、46g乙醇所含的羟基的电子数是7NA |
| C、2.3g Na与足量O2反应,生成Na2O和Na2O2的混合物,钠共失去0.1NA个电子 |
| D、18g葡萄糖分子中含有共用电子对数为2.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com