
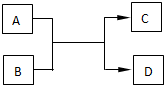
 学习了元素周期表,可以帮助我们进一步丰富不同元素间的相互转化关系.已知A、B、C、D都处于短周期,A、D为单质,B、C是化合物.
学习了元素周期表,可以帮助我们进一步丰富不同元素间的相互转化关系.已知A、B、C、D都处于短周期,A、D为单质,B、C是化合物.分析 A、D为短周期单质,B、C是短周期元素的化合物,说明该反应为置换反应.
(1)假设A、D元素处于同主族:
①当B是H2O时,应为钠和水的反应,生成氢氧化钠和氢气;
②当B、C均为氧化物时,应为C和二氧化硅的反应;
(2)假设A、D不在同主族:
①当B是H2O且B是还原剂时,被氧化生成氧气,应为氟气和水的反应;
②当B是H2O且B是氧化剂时,生成氢气,可为C和水的反应.
解答 解:A、D为短周期单质,B、C是短周期元素的化合物,说明该反应为置换反应,
(1)假设A、D元素处于同主族:
①当B是H2O时,应为钠和水的反应,生成氢氧化钠和氢气,方程式为2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;
②当B、C均为氧化物时,应为C和二氧化硅的反应,方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO,工业上利用该反应制粗硅,
故答案为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO;制粗硅;
(2)假设A、D不在同主族:
①当B是H2O且B是还原剂时,被氧化生成氧气,应为氟气和水的反应,方程式为2F2+2H2O=4HF+O2↑,
故答案为:2F2+2H2O=4HF+O2↑;
②当B是H2O且B是氧化剂时,生成氢气,可为C和水的反应,方程式为C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2,
故答案为:C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2.
点评 本题考查无机物的推断,属于开放性题目,考查综合运用知识的能力,注意掌握中学常见的置换反应,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
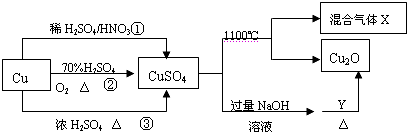
| A. | 1mol CuSO4在1100℃所得混合气体X中O2可能为0.75mol(X的组成为SO2、SO3、O2) | |
| B. | 相对于途径①、②,途径③更好地体现了绿色化学理念 | |
| C. | 途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 | |
| D. | Y一定是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ②③ | C. | ①② | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同一元素不可能既表现金属性,又表现非金属性 | |
| B. | 第三周期元素的最高正化合价等于它所处的主族序数 | |
| C. | 短周期中同主族元素的最外层电子数及化学性质完全相同 | |
| D. | 同周期元素的原子半径从左到右依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油是混合物,其分馏产品汽油为纯净物 | |
| B. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| C. | 金属氧化物均为碱性氧化物 | |
| D. | “血液透析”利用了胶体的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
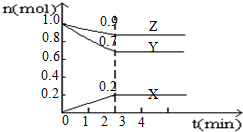 某温度时,在4L的容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在4L的容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
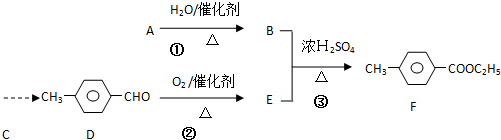
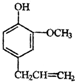 )是一种重要的调味剂,它与F的关系是b(填序号).
)是一种重要的调味剂,它与F的关系是b(填序号).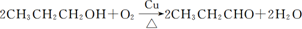 ,氧化反应;
,氧化反应;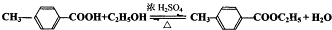 ,取代反应(或酯化反应).
,取代反应(或酯化反应).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com