
将4.6g Na投入到95.6g水中,所得溶液中溶质的质量分数为( )
A. 小于4.6% B. 等于8.0% C. 小于8.0% D. 大于8.0%
考点: 化学方程式的有关计算.
专题: 计算题.
分析: 钠投入到水中,发生2Na+2H2O=2NaOH+H2↑,根据反应的化学方程式计算生成NaOH的质量和氢气的质量,溶液的质量=m(Na)+m(水)﹣m(氢气),进而计算溶质的质量分数.
解答: 解:将4.6g钠投入到95.4g水中,发生2Na+2H2O=2NaOH+H2↑,则:
2Na+2H2O=2NaOH+H2↑
46g 80g 2g
4.6g m(NaOH) m(H2)
m(NaOH)=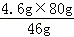 =8.0g,
=8.0g,
m(H2)=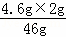 =0.2g,
=0.2g,
故溶液质量为4.6g+95.6g﹣0.2g=100g,
则w(NaOH)= ×100%=8%,
×100%=8%,
故选B.
点评: 本题考查溶液质量分数的计算、化学方程式计算,题目难度不大,注意计算溶液的总质量.


科目:高中化学 来源: 题型:
(1)有以下八种饱和溶液:①Ba(NO3)2;②Ca(OH)2;③Ca(ClO)2;④CaCl2;
⑤Na2CO3;⑥NaAlO2;⑦NH3和NaCl;⑧Na2SiO3.向其中分别持续通入CO2,最终能得到沉淀或析出晶体的是 (请填序号)
(2)氯化铵水溶液显酸性,请用离子方程式表示原因 ;
如往氯化铵浓溶液中加入镁粉,反应剧烈且放出气体能使湿润红色石蕊试纸变蓝色,请写出相应离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2下列说法正确的是( )
A. SO2既是氧化产物又是还原产物
B. CuFeS2仅作还原剂,硫元素被氧化
C. 每生成1 molCu2S,有4mol硫被氧化
D. 每转移1.2 mol电子,有0.2 mol硫被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
某探究小组在实验室中用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝.回答下列问题:
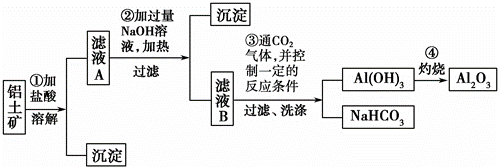
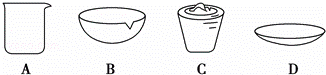
(1)在实验中需用1mol•L﹣1的NaOH溶液480mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器 .在灼烧操作中用到下列仪器中的一种,其名称是 .
写出步骤①中发生反应的离子方程式 .
(3)操作③中的洗涤操作如何进行? .
(4)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象.
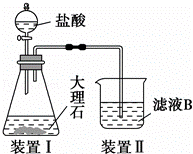
乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理? .若合理,请用离子方程式解释其原因 (若你认为不合理,该空不作答).
丙同学分析认为:甲同学通入的CO2中含有HCl气体,也是导致实验失败的原因,在实验中增加某装置可解决这个问题.请帮助丙同学画出该装置图,并注明试剂名称.
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 64g SO2中含有的氧原子数为2NA
B. 含有6.02×1023个H原子的H2在标准状况下的体积约为22.4L
C. 40g NaOH溶解在1L水中,所制得的溶液,物质的量浓度为1mol•L﹣1
D. 标准状况下,11.2L H2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 纯碱和生石灰都属于碱
B. 干冰和氨都属于弱电解质
C. 沼气和乙醇都属于可再生能源
D. 铝和铜在工业上都常用电解法冶炼
查看答案和解析>>
科目:高中化学 来源: 题型:
与纯水的电离相似,液氨中也存在着微弱的电离:
2NH3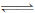
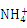 +
+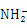 ,据此判断以下叙述中错误的是
,据此判断以下叙述中错误的是
A.液氨中含有NH3、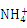 、
、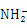 等微粒
等微粒
B.一定温度下液氨中c(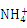 )•c(
)•c(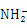 )是个常数
)是个常数
C.液氨的电离达到平衡时:c(NH3)= c(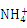 )=c(
)=c(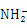 )
)
D.只要不加入其他物质,液氨中c(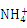 )=c(
)=c(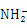 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A依次减小,B和E同主族.
下列推断不正确的是( )
|
| A. | A、B、E一定在不同周期 |
|
| B. | C的最高价氧化物的水化物可能显碱性 |
|
| C. | A、D可能在同一主族 |
|
| D. | C和D的单质可能化合形成离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com