
【题目】已知下列实验事实:
①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;
②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液;
③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
A. 化合物KCrO2中Cr元素为+3价
B. 实验①证明Cr2O3是两性氧化物
C. 实验②证明H2O2既有氧化性又有还原性
D. 实验③证明氧化性: Cr2O72-> I2
科目:高中化学 来源: 题型:
【题目】分析下列反应回答相应问题.
①3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
未被还原的硝酸与参加反应的总硝酸的质量比为 .
②S+2KNO3+3C ![]() K2S+N2↑+3CO2↑ 还原剂是还原产物是
K2S+N2↑+3CO2↑ 还原剂是还原产物是
③3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移mol电子.
5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移mol电子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度均为0.100mol/L的下列物质的溶液中,c(NH4+)最大的是( )
A.NH4ClB.NH4HSO4C.NH3·H2OD.CH3COONH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为了验证CH4是否具有还原性,设计了如下实验:
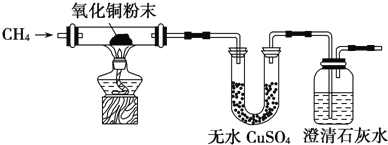
(1)实验过程中观察到无水CuSO4逐渐变蓝,澄清石灰水出现浑浊现象,则CH4与CuO反应的化学方程式为________________________________;
(2)研究小组将CH4通入溴水时,发现溴水逐渐褪色,你认为原因可能是___________________;请设计一个实验方案证明你的结论(用文字表示,不必画实验装置图)_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,回答下列问题:
(1)还原产物是
(2)氧化剂与还原剂的物质的量之比是
(3)用双线桥标上电子转移的方向和数目 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
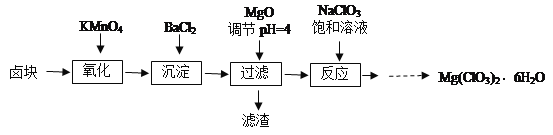
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S )随温度(T )变化曲线如图所示。
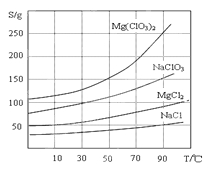
回答下列问题:
(1)调pH时,加入MgO的原因___________。
(2)加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀完全?____________。
(3)加入NaClO3饱和溶液后发生反应的类型为_____________________________,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:蒸发浓缩、①______;②_____;③过滤、洗涤。
(4)产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量4.00 g产品配成100 mL溶液。
步骤2:取10 mL于锥形瓶中,加入10 mL稀硫酸和30 .00mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol·L-1K2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液30.00 mL。
①滴定时应用_____________(“酸式”或“碱式”)滴定管。步骤2中发生反应的离子方程式:_____________________________。
②产品中Mg(ClO3)2·6H2O的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KI+5KIO3+3H2S=3I2+3K2SO4+3H2O,下列说法正确的是( )
A.氧化剂和还原剂物质的量之比为5:4
B.3 mol H2S可还原4mol的KIO3
C.I2是还原产物,K2SO4是氧化产物
D.1molKIO3可氧化0.2mol的KI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅及其化合物广泛用于蓄电池、机械制造、电缆护防等行业。
(1)用PbS熔炼铅的过程中会有如下反应发生:
2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) △H=a kJ·mol-1
PbS(s) +2O2(g) =PbSO4(s) △H=b kJ·mol-1
PbS(s) +2PbO(s) =3Pb(s) +SO2(g) △H=c kJ·mol-1
写出PbS与PbSO4反应生成Pb和SO2的热化学方程式____________________。
(2)利用电解法也可制得金属铅。将PbO溶解在HCl和NaCl的混合溶液中,得到含[PbC14]2-的电解液。用惰性电极电解Na2PbCl4溶液制得金属Pb,装置如下图所示。

a电极的名称是__________,b电极的电极反应式为______________________,该生产过程中可以循环利用的物质是____________________。
(3)铅蓄电池是一种用途广泛的二次电池。铅蓄电池的电池反应通常表示如下:Pb+PbO2+2H2SO4![]() 2PbSO4 +2H2O。铅蓄电池充电时,二氧化铅电极应与外接电源的_________________(填“正极”或“负极”)相连接,该电极的电极反应式为________________________________。
2PbSO4 +2H2O。铅蓄电池充电时,二氧化铅电极应与外接电源的_________________(填“正极”或“负极”)相连接,该电极的电极反应式为________________________________。
(4)PbO2受热会随温度升高逐步分解。称取23.9g PbO2,将其加热分解,受热分解过程中固体质量随温度的变化如下图所示。

A点与C点对应物质的化学式分别为____________、_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com