
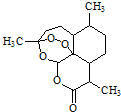
| A. | 青蒿素分子式为C15H20O5 | |
| B. | 可用蒸馏水提取植物中的青蒿素 | |
| C. | 青蒿素在碱性条件下易发生水解反应 | |
| D. | 青蒿素遇湿润的淀粉碘化钾试纸立刻显蓝色,是因为分子结构中含有酯基 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:选择题
下列有关环境问题的做法错误的是
A.生活污水使用明矾杀菌消毒 B.向燃煤中加入适量石灰石“固硫”
C.推广使用可降解塑料防止白色污染 D.提倡公交出行可减少氮氧化物排放
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
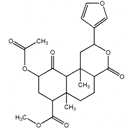
| A. | 分子中含有6个手性碳原子 | |
| B. | 能使酸性高锰酸溶液褪色 | |
| C. | 1mol该有机物最多可与含3molNaOH的水溶液反应 | |
| D. | 1mol该有机物最多可与3molH2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4 L乙烯中C-H键数为4NA | |
| B. | 1 mol羟基中电子数为10NA | |
| C. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA | |
| D. | 常温下,1 L 0.1 mol•L-1 的NH4NO3溶液中氮原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
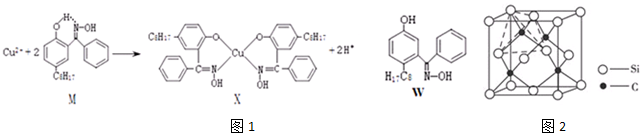
| A. | 元素非金属性由强到弱的顺序:Z、W、X | |
| B. | 原子半径由大到小的顺序:W、Z、Y、X | |
| C. | 原子最外层电子数由多到少的顺序:Y、X、W、Z | |
| D. | 简单气态氢化物的稳定性由强到弱的顺序:X、Y、W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ① | C. | ④ | D. | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com