
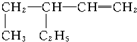 名称:3-乙基-1-戊烯.
名称:3-乙基-1-戊烯. 名称:5-甲基-2-己烯.
名称:5-甲基-2-己烯. 名称:5-甲基-3-庚炔.
名称:5-甲基-3-庚炔. 分析 (1)、(2)烯烃命名中选取含有碳碳双键的最长碳链,距离双键最近的一端为1号碳;
(3)炔烃命名中选取含有碳碳三键的最长碳链,距离三键最近的一端为1号碳,据此解答即可.
解答 解:(1)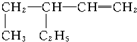 含有碳碳双键的最长碳链为5,从右端命名,在3号碳上含有1个乙基,碳碳双键在1、2号碳之间,正确命名为:3-乙基-1-戊烯,故答案为:3-乙基-1-戊烯;
含有碳碳双键的最长碳链为5,从右端命名,在3号碳上含有1个乙基,碳碳双键在1、2号碳之间,正确命名为:3-乙基-1-戊烯,故答案为:3-乙基-1-戊烯;
(2) 含有碳碳双键的最长碳链为6,从由端命名,在5号碳上含有1个甲基,碳碳双键在2、3号碳之间,正确命名为:5-甲基-2-己烯,故答案为:5-甲基-2-己烯;
含有碳碳双键的最长碳链为6,从由端命名,在5号碳上含有1个甲基,碳碳双键在2、3号碳之间,正确命名为:5-甲基-2-己烯,故答案为:5-甲基-2-己烯;
(3) 含有碳碳三键的最长碳链为7,从右端命名,碳碳三键在3、4号碳之间,正确命名为:5-甲基-3-庚炔,故答案为:5-甲基-3-庚炔.
含有碳碳三键的最长碳链为7,从右端命名,碳碳三键在3、4号碳之间,正确命名为:5-甲基-3-庚炔,故答案为:5-甲基-3-庚炔.
点评 本题主要考查的是烯烃和炔烃的命名,熟练掌握烷烃的命名原则,依据烷烃的命名法则,结合碳碳双键或三键的位置命名即可,难度不大.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:解答题

| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.3000 | 1.02 | 24.04 |
| 2 | 0.3000 | 2.00 | 25.03 |
| 3 | 0.3000 | 0.20 | 23.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中N-C-N键角为90° | |
| B. | C(N3)4中碳元素为正价,C(N3)4分子中存在极性键和非极性键 | |
| C. | C(N3)4就是石墨吸附N2后所得的物质 | |
| D. | 该物质为分子晶体,每18g C(N3)4完全分解可产生13.44L的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClO2的分子结构呈V型,属非极性分子 | |
| B. | ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以单位体积得电子的数目表示)是Cl2的5倍 | |
| C. | ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害 | |
| D. | 常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3+2NaClO3+H2SO4═2Na2SO4+2ClO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在此反应中硝酸体现强氧化性,全部被还原 | |
| B. | 向反应后的溶液中再加入金属铁,不再发生化学反应 | |
| C. | 该反应中被还原的硝酸与未被还原的硝酸之比为1:4 | |
| D. | 该反应中被还原的硝酸与未被还原的硝酸之比为1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com