
| A. | 硫酸溶液 | B. | 氨水溶液 | C. | 盐酸溶液 | D. | 氢氧化钠溶液 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s) 盐桥(盛有KNO3琼脂的U型管)构成一个原电池设计的原电池如图所示,盐桥(盛有KNO3琼脂的U型管).请回 答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s) 盐桥(盛有KNO3琼脂的U型管)构成一个原电池设计的原电池如图所示,盐桥(盛有KNO3琼脂的U型管).请回 答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
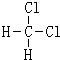 和
和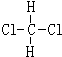 ⑤40K和40Ca ⑥
⑤40K和40Ca ⑥ 与
与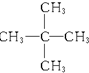 ⑦甲烷与C3H8.
⑦甲烷与C3H8.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅的单质都可用作半导体材料 | B. | 石英可用来制造光导纤维 | ||
| C. | 碳化硅可用作砂纸、砂轮的磨料 | D. | 水玻璃可作黏合剂及耐火材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第15列元素的最高价氧化物的化学式为R2O5 | |
| B. | 第2列元素中肯定没有非金属元素 | |
| C. | L层电子数为奇数的所有元素所在族的序数与元素原子L层电子数相等 | |
| D. | M层电子数为奇数的所有元素所在族的序数与元素原子M层电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
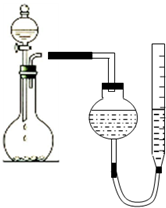 某学生用图所示的装置测定镁的相对原子质量:
某学生用图所示的装置测定镁的相对原子质量:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
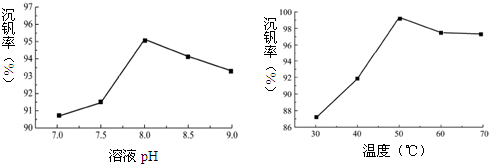
| 实验步骤与结论: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 上下移动①中铜丝可控制生成SO2的量 | |
| B. | ②中选用品红溶液验证SO2的生成 | |
| C. | ③中选用NaOH溶液吸收多余的SO2 | |
| D. | 该反应中浓硫酸表现了强氧化性和脱水性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com