
 ��ֱ��úȼ�ϵ�ء��ܹ���ú�еĻ�ѧ�ܸ�Ч������ת��Ϊ���ܣ�������Na2CO3������ʵ�ֱ��úȼ�ϵ�صĹ���ԭ����ͼ�������й�˵����ȷ���ǣ�������
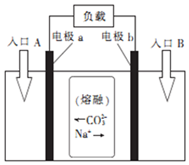
��ֱ��úȼ�ϵ�ء��ܹ���ú�еĻ�ѧ�ܸ�Ч������ת��Ϊ���ܣ�������Na2CO3������ʵ�ֱ��úȼ�ϵ�صĹ���ԭ����ͼ�������й�˵����ȷ���ǣ�������| A�� | �õ�ص��ܷ�ӦΪC+O2�TCO2 | |
| B�� | úֱ��ȼ�շ����ֱ��úȼ�ϵ�ط�������������ʸ� | |
| C�� | ���뷴Ӧ�ҵ�ú�����ɷ�ĩ״�Է�Ӧ���ʺ��Ⱦ���Ӱ�� | |
| D�� | �����ɵ缫b�ص�������缫a�����A���������Ϊú�� |
���� ȼ�ϵ���У���������������������������������a�Ǹ�����Ϊ����ȼ��C�ĵ缫��b��������ͨ��������O2�ĵ缫�������Ϊ����̼���ƣ�����ӦʽΪC-4e-+2CO32-=3CO2��������ӦʽΪO2+4e-=2O2-����ط�ӦʽΪC+O2�TCO2���ŵ�ʱ�����ӴӸ����ص��������������ݴ˷������
��� �⣺A��ͨ�����Ϸ���֪����ط�ӦʽΪC+O2�TCO2����A��ȷ��
B��úȼ�ϵ���ܽ���ѧ��ֱ��ת��Ϊ���ܣ���úȼ�շ���ʱ��ת��Ϊ������ת��Ϊ���ܣ�����úȼ�ϵ�ر�úֱ��ȼ�շ������������ʸߣ���B����
C�����뷴Ӧ�ҵ�ú�����ɷ�ĩ״��ӿ췴Ӧ���ʣ�������Ӱ�죬��C����
D��ͨ�����Ϸ���֪��a�Ǹ�����b�����������ӴӸ���a�ص�����������b�����A���������Ϊú�ۣ���D����
��ѡA��
���� ���⿼�黯ѧ��Դ���͵�أ�Ϊ��Ƶ���㣬��ȷԭ���ԭ���ǽⱾ��ؼ���֪���������жϷ�������������ط�Ӧʽ����д���ɽ�𣬵缫��Ӧʽ����дҪ��ϵ�����ص㣬ע��÷�Ӧ�����Ϊ����״̬̼���ƣ�


 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
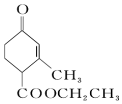 ��
��  ��ǰ�߲������Ĺ�����Ϊ��д�ṹ��ʽ���ʻ������������߹������У�д���ƣ��������ǻ���
��ǰ�߲������Ĺ�����Ϊ��д�ṹ��ʽ���ʻ������������߹������У�д���ƣ��������ǻ���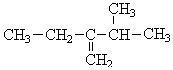 ������Ϊ3-��-2-�һ�-1-��ϩ��
������Ϊ3-��-2-�һ�-1-��ϩ��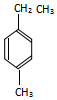 ������Ϊ�Լ��ұ���
������Ϊ�Լ��ұ���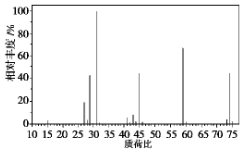
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
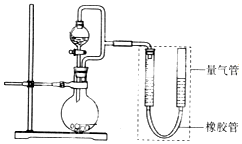 ��2L�����ܱ������У�������Ӧ 2NO��g��+O2��g��?2NO2��g����
��2L�����ܱ������У�������Ӧ 2NO��g��+O2��g��?2NO2��g����| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ǻ��ĵ���ʽ��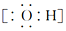 | B�� | ����ķ���ʽ��CH3COOH | ||
| C�� | ������Ľṹ��ʽ��CH2BrCH2Br | D�� | ��Ȳ��ʵ��ʽ��CH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | �������� |
| A | ����м����ˮ������ϼ��� | ��ȡ�屽 |
| B | �ȼ���Ũ���ᣬ�ټ��뱽��������Ũ���� | ��ȡ������ |
| C | ��C6H5ONa��Һ��ͨ��CO2���� | ��Һ���ֻ��ǣ�֤�����ԣ�C6H5OH��H2CO3 |
| D | �Ҵ���Ũ�����ϼ��ȣ�������������ͨ�����Ը��������Һ�� | ���Ը��������Һ��ɫ��֤���Ҵ�������ȥ��Ӧ������ϩ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ�ص��������������������� | |
| B�� | ��ѧ���Ǵ����ڷ��ӡ�ԭ�Ӻ����Ӽ�������� | |
| C�� | ԭ�ӵ�������ԭ�Ӻ�������������������ͬ���� | |
| D�� | ��ѧ��Ӧ���ʿ��Ծ�����Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | W��X��Y��Z����������֮��Ϊ20 | B�� | WX2��YX2��ZX2��ֻ�����ۼ� | ||
| C�� | ԭ�Ӱ뾶�Ĵ�С˳��ΪX��W��Y��Z | D�� | Z����̬�⻯���Y���ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��������������
��������������  ��Ϊͬ���칹����ǣ�������
��Ϊͬ���칹����ǣ�������| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ����Ϊ890.3KJ•mol-1�������ȼ���ȵ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3 kJ•mol-1 | |
| B�� | 500�桢30 MPa �£���0.1 mol N2 �� 0.3 mol H2 �����ܱ������г�ַ�Ӧ����NH3��g��������3.86 KJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��$?_{500��30MPa}^{����}$ 2NH3��g����H=-38.6 KJ•mol-1 | |
| C�� | ��֪1 gҺ̬�º�����Һ̬�������ⷴӦ���ɵ�����ˮ����ʱ�ų�20.05 kJ���������º������ⷴӦ���Ȼ�ѧ����ʽΪ�� N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.6 KJ•mol-1 | |
| D�� | CO��g����ȼ������283.0 KJ•mol-1����2CO2��g���T2CO��g��+O2��g�� ��Ӧ�ġ�H=+283.0 KJ•mol-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com