
��1��AgNO3+NaCl=NaNO3+AgCl�� ��2��2AgCl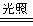 2Ag+Cl2��
2Ag+Cl2��
��3��3Cl2+3H2O=5HCl+HClO3 ��4��HCl+AgNO3=AgCl��+HNO3
�������ɵ�Ag�����ʵ���Ϊx���ɷֽ��ʿ�֪�����ɵ�AgClΪ9x�����ɷ�Ӧ�Ļ�ѧ����ʽ����ԭ���غ㣬������ԭ��ֻ������AgCl��HClO3�С����ԣ�9x+x/6��mol=1.1mol��n��Ag��=0.12mol��n��AgCl��=1.08mol���Ӷ��ó�m����=168g��
c��H+��=0.12mol��1.2L=0.1mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1�� |
|
| ����2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���dz����⡤�̲�ȫ��ȫ�������л�ѧ������1��(ɽ����) ɽ���� ���ͣ�038
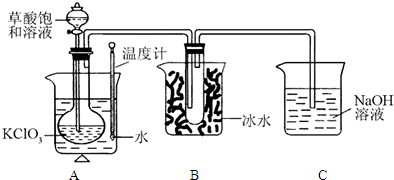
��֪KClO3��Һ�����ԣ�Cl����Ag+��Ӧ����AgCl��ÿ�������ɵ�AgCl����10��(��������)����ֽ�ɵ���������������������ˮ���绯��HClO3(ǿ��)��HCl��HCl�е�Cl������ʣ���Ag+��Ӧ���ɳ��������ѭ��������ֱ�����ˣ�
(1)д������������Ӧ���ܻ�ѧ����ʽ��
(2)����1 mol��NaCl����Һ�м���������AgNO3��Һ���ʣ����������ɶ��ٿ�������(Ag��AgCl)�������������Һ�����Ϊ1.2 L������Һ��H+Ũ���Ƕ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�γ��ϸԸ���ѧ2007�����ڶ��νο��ԡ���ѧ���� ���ͣ�022
| |||||||||||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㶫ʡģ���� ���ͣ�ʵ����


�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com