
“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是()
A. 构造原理 B. 泡利原理 C. 洪特规则 D. 能量最低原理
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
FeCl3、CuCl2的混合溶液中加入铁粉,充分应后仍有固体存在,下列判断不正确的是( )
|
| A. | 加入KSCN溶液一定不变红色 | B. | 溶液中一定含Fe2+ |
|
| C. | 溶液中一定含Cu2+ | D. | 剩余固体中一定含铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对CH3﹣CH=CH﹣C≡C﹣CF3分子结构的下列叙述中,正确的是( )
|
| A. | 6个碳原子有可能都在同一直线上 |
|
| B. | 在同一直线上的原子至少有5个 |
|
| C. | 在同一平面上的原子至少有8个 |
|
| D. | 分子中呈四面体结构的碳原子有3个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为: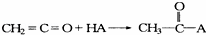 ,乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是( )
,乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是( )
|
| A. | 与HCl加成生成CH3COCl |
|
| B. | 与H2O加成生成CH3COOH |
|
| C. | 与CH3OH加成生成CH3COCH2OH |
|
| D. | 与CH3COOH加成生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
物质A有如下反应路线:
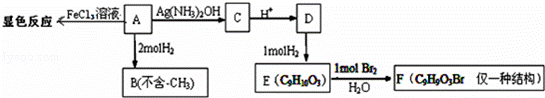
(1)1mol 物质A最多能消耗H2的物质的量为
(2)A→C的化学方程式为 ;
(3)H、G与B互为同分异构,且满足下列条件:①H、G与浓溴水和NaHCO3都不反应,且结构中均不含有﹣CH3(官能团不能同时连在同一个碳原子上). ②1molH、G 都能与2molNa反应. ③H环上一氯取代只有2种,G环上一氯取代只有3种.
H的结构简式为 ;G的一种结构简式为 .
(4)已知在一定条件下R1CH=CHR2→R1CHO+R2CHO,A在一定条件下氧化生成羧酸X、Y.X是芳香族化合物,Y是一种还原性的二元羧酸.
写出X在浓硫酸条件下的缩聚反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于主族元素电子排布特征的说法正确的是()
A. 主族元素的原子核外电子最后填入的能级是s能级
B. 主族元素的原子核外电子最后填入的能级是s能级或p能级
C. 主族元素的原子核外电子最后填入的能级是d能级或f能级
D. 主族元素的原子核外电子最后填入的能级是s能级或d能级
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下,下列物质占体积最大的是()
A. 0.6 g H2 B. 98 g H2SO4
C. 6.02×1022个CO2 D. 4.48 L HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
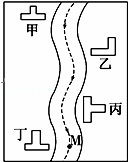
某小河边有四座工厂:甲、乙、丙、丁(如图所示).已知,它们所排出的废液里分别含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某环保小组对河水监测时发现:①甲处河水呈乳白色②乙处河水呈红褐色浑浊状③丙处河水由浑浊变清④丁处河水产生气泡,河水仍澄清.
请推断:
(1)四座工厂排出的废液里含有的污染物是甲 ,乙 ,丙 ,丁 .
在M处取出的河水中,肯定大量存在的离子有 .
(3)用离子方程式表示丙除河水变澄清的原因: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com