
| A.只增大c(A)时,v也增大 | B.只增大c(A)时,v值不变 |
| C.只升高温度时,k值不变 | D.只升高温度时,k值变小 |
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:不详 题型:单选题
| A.升高温度 | B.加大x的投入量 |
| C.增大体积 | D.加催化剂 |
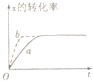
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.K=
| ||
| B.K值越大表示达到平衡时,正反应进行程度越大 | ||
| C.其它条件不变时,温度升高,K值增大 | ||
| D.其它条件不变时,压强减小,K值减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学平衡常数越大,说明该反应进行得越完全 |
| B.可逆反应达到化学平衡状态后,改变外界条件不会改变平衡状态 |
| C.化学反应中,物质含有的活化分子数目越多,化学反应速率越快 |
| D.可逆反应维持的时间越长,生成物的百分含量必定越高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.①②④ | C.②③④ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| CO的初始浓度(mol/L) | 2 | 4 | 1 | 3 |
| H2的初始浓度(mol/L) | 3 | 2 | 3 | 3 |
| 时间(min) | 8 | 6 | 12 | n |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.变深 | B.变浅 | C.不变 | D.无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com