
 .
. 分析 (1)反应中元素化合价不变,不属于氧化还原反应;
(2)中Fe元素化合价由0价变为+2价、H元素化合价由+1价变为0价,所以属于氧化还原反应,转移电子数为2.
解答 解:(1)BaCl2+Na2SO4═BaSO4↓+2NaCl反应中各元素化合价不变,不属于氧化还原反应,属于复分解反应;
故答案为:不是氧化还原反应;
(2)Fe+2HCl═FeCl2+H2↑中Fe元素化合价由0价变为+2价、H元素化合价由+1价变为0价,所以属于氧化还原反应,转移电子数为2,转移电子方向和数目为 ,
,
故答案为: .
.
点评 本题考查氧化还原反应判断、电子转移方向和数目的书写,侧重考查基本概念,熟悉常见元素化合价变化,知道氧化还原反应本质和特征的区别.


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:选择题
 如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )
如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )| A. | X的平衡转化率为85% | |
| B. | 第6 min 后,反应就终止了 | |
| C. | 若升高温度,X的平衡转化率将大于85% | |
| D. | 若降低温度,v正减小,v逆增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
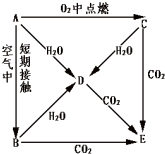 A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,己知A金属为单质.
A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,己知A金属为单质.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | M的单质可用于从钛、锆等金属的氯化物溶液中置换出钛、锆等单质 | |
| B. | 由X、Y、Z三种元素形成的某种化合物的水溶液,可能呈碱性或酸性 | |
| C. | 由X、M与Z形成的化合物X2Z2和M2Z2中所含的化学键类型相同 | |
| D. | 含有W阳离子的某种盐,可用作净水剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com