
 ��X�ĵ���ʽ��
��X�ĵ���ʽ�� ��Bת��ΪC�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O��
��Bת��ΪC�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O�� ��
������ ��1��X������10��������1��1��������ˮ��Һ��ʹ��̪��죬��XΪNaOH����A���ɵ�������2��Ԫ�ذ�1��3��ɵ��Σ���AΪAlCl3��BӦΪAl��OH��3��CΪNaAlO2��
��2��������A��B��C��X��Ϊ��̬���ʣ�1molA�к��й��ۼ�����ĿԼΪ1.806��1024��ӦΪNH3��XΪ���ʣ�ӦΪO2��BΪNO��CΪNO2��
��3��AΪ�����ڵ��ʣ���AԪ�ص�ԭ�ӵ��������������۵Ĵ�����Ϊ6����AΪCl2��XΪĿǰʹ����㷺���������Ľ������ʼ�ΪFe����BӦΪFeCl3��CΪFeCl2��
��� �⣺��1��X������10��������1��1��������ˮ��Һ��ʹ��̪��죬��XΪNaOH����A���ɵ�������2��Ԫ�ذ�1��3��ɵ��Σ���AΪAlCl3��BӦΪAl��OH��3��CΪNaAlO2����������A��B��C����������Ԫ��RΪAl����R�������ӵĽṹʾ��ͼΪ�� ��X�ĵ���ʽ�ǣ�
��X�ĵ���ʽ�ǣ� ��Bת��ΪC�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O��
��Bת��ΪC�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ�� ��
�� ��Al��OH��3+OH-=AlO2-+2H2O��
��Al��OH��3+OH-=AlO2-+2H2O��
��2��������A��B��C��X��Ϊ��̬���ʣ�1molA�к��й��ۼ�����ĿԼΪ1.806��1024��ӦΪNH3��XΪ���ʣ�ӦΪO2��BΪNO��CΪNO2����A��X��Ӧ����B�Ļ�ѧ����ʽ��4NH3+5O2$\frac{\underline{\;����\;}}{��}$4NO+6H2O��A�ĽṹʽΪ ��
��
�ʴ�Ϊ��4NH3+5O2$\frac{\underline{\;����\;}}{��}$4NO+6H2O�� ��
��
��3��AΪ�����ڵ��ʣ���AԪ�ص�ԭ�ӵ��������������۵Ĵ�����Ϊ6����AΪCl2��XΪĿǰʹ����㷺���������Ľ������ʼ�ΪFe����BӦΪFeCl3��CΪFeCl2������X�����ڱ��е�λ��Ϊ�������ڢ����壬B��X��Ӧ�����ӷ���ʽΪFe+2Fe3+=3Fe2+���ʴ�Ϊ���������ڢ����壻Fe+2Fe3+=3Fe2+��
���� ���⿼��������ƶϣ���Ŀ�ѶȲ���ע����������Ϣ������ת����ϵ�жϷ�Ӧ���ص㣬������ʵĹ��ɺ������ƶ����ʵ����࣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ������ͺ�ˮ ������ͺ�ˮ | B�� | 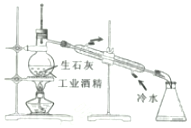 �ù�ҵ�ƾ���ȡ��ˮ�ƾ� �ù�ҵ�ƾ���ȡ��ˮ�ƾ� | ||
| C�� | 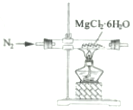 ��ȡMgCl2���� ��ȡMgCl2���� | D�� | 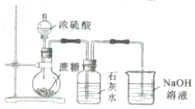 ���������Ũ���ᷴӦ������CO2 ���������Ũ���ᷴӦ������CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
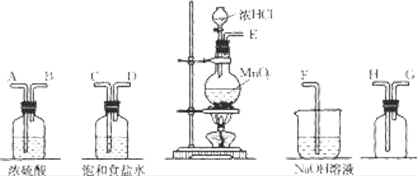
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

| ʵ�鲽�� | ʵ������ | �û�ѧ������� |
| ����������ͨ�����KI��Һ | ��Һ��������ɫ | Cl2+2I-=I2+2Cl-�������ӷ���ʽ��ʾ�� |
| ����ͨ������ | ��Һ�����ɫ | 5Cl2+I2+6H2O=2HIO3+10HCl���û�ѧ����ʽ��ʾ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
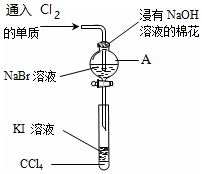 Ϊ����֤VIIA�岿��Ԫ�طǽ����Եݱ���ɣ������ͼ����ʵ�飬
Ϊ����֤VIIA�岿��Ԫ�طǽ����Եݱ���ɣ������ͼ����ʵ�飬�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
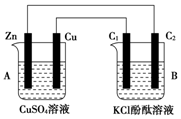 ��ͼ��ʾװ�ý���ʵ�飬���ش��������⣺
��ͼ��ʾװ�ý���ʵ�飬���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʯ��ˮ��ͨ������Ķ�����̼CO2+OH?�THCO3- | |
| B�� | �����ƺ�ˮ��Ӧ2Na+2H2O�T2Na++2OH-+H2�� | |
| C�� | �����Ȼ�������Һ�м���˫��ˮ2Fe2++H2O2�T2Fe3++O2��+2H+ | |
| D�� | �����������Ȼ�����Һ���ɳ����ķ�ӦSO3+Ba2++H2O�TBaSO4��+2H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Mg��Al��Cu�ڿ����г�ʱ����ã������������������� | |
| B�� | ��SO2����ֱ�ͨ�뵽BaCl2��Ba��NO3��2��Һ�о��а�ɫ�������� | |
| C�� | ��ҵ��ͨ���õ���ơ�þ������Ӧ�������Ȼ����Ƶø����ֽ������� | |
| D�� | ��ˮ����ͨ�����ȵ����ۣ���Ӧ������������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com