
| A、(100-3a)% | ||
B、
| ||
C、
| ||
D、
|
| 1 |
| 3 |
| 100-a |
| 3 |


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
| A、只有① | B、只有③ |
| C、①和③ | D、②和③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯分子是碳碳单双键交替相连的结构,因此苯环上碳碳键的键长都不相等 |
| B、甲烷分子是以碳原子为中心的四面体结构,CCl4却不是正四面体结构 |
C、 属于脂环化合物 属于脂环化合物 |
| D、苯是一种无色液体,难溶于水,密度比水小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石英(SiO2)是制造玻璃的重要原料之一 |
| B、石英砂可以用于制取高纯度的硅,硅是将太阳能转化为电能的常用材料 |
| C、Na2SiO3是制备硅胶和木材防火剂的原料 |
| D、晶体硅是制造光导纤维的材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5所指颗粒物大小与胶体中分散质粒子大小相当 |
| B、O2和O3互为同素异形体,两者的化学性质相同 |
| C、O3转化为O2和O2转化为O3过程中均有能量变化 |
| D、反应3O2=2O3有单质参加,属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3溶液中加入NaOH 溶液:HCO3-+OH-═CO2↑+H2O |
| B、在NaOH溶液中滴入少量AlCl3溶液:Al3++3OH-═Al(OH)3↓ |
| C、甲酸溶液中滴入NaOH溶液:HCOOH+OH-═HCOO-+H2O |
| D、CO2通入CaCl2溶液:CO2+H2O+Ca2+═CaCO3↓+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.104 | 0.111 | 0.066 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、R的氧化物及其对应的水化物均具有两性 |
| B、L、M的单质均用电解其熔融盐的方法冶炼 |
| C、T的氢化物还原性及稳定性均比Q的氢化物强 |
| D、五种元素的常见简单离子中半径最大的是Q2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
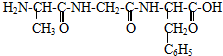
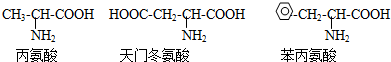
| A、D-12 | ||
| B、D-13 | ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| A | 该元素有一种核素质量数为1 |
| B | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| C | 形成的简单离子是第三周期元素形成简单离子半径中最小的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com