
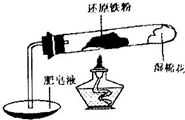
 铁不能与冷、热水反应,但能与水蒸气反应.中学教材中用下图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.
铁不能与冷、热水反应,但能与水蒸气反应.中学教材中用下图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,加入盐酸,微热. | 黑色粉末逐渐溶解,有少量气泡产生. |
| ② | 取试管1反应后的溶液少许,滴加几滴KSCN溶液,振荡. | 溶液没有出现血红色. |
| ③ | 取试管1反应后的溶液少许,滴加几滴酸性KMnO4溶液,振荡 | 高锰酸钾溶液褪色 |

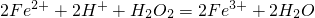 ,
,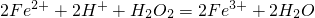 ;
;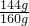 =0.9;
=0.9;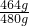 =0.97,m1与m2之比最少应大于 0.9时,固体样品中一定存在Fe3O4,故答案为:0.9.
=0.97,m1与m2之比最少应大于 0.9时,固体样品中一定存在Fe3O4,故答案为:0.9.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈绿色;有少量气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
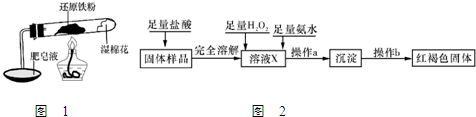
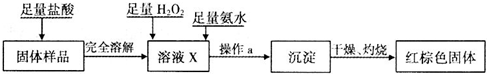
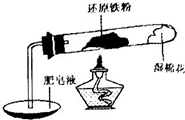 铁不能与冷、热水反应,但能与水蒸气反应.中学教材中用下图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.
铁不能与冷、热水反应,但能与水蒸气反应.中学教材中用下图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,加入盐酸,微热. | 黑色粉末逐渐溶解,有少量气泡产生. |
| ② | 取试管1反应后的溶液少许,滴加几滴KSCN溶液,振荡. | 溶液没有出现血红色. |
| ③ | 取试管1反应后的溶液少许,滴加几滴酸性KMnO4溶液,振荡 | 高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)铁不能与冷、热水反应,但能与水蒸气反应。如下图所示,在装置的硬质玻璃管内放入还原铁粉和石棉绒的混合物,通入水蒸气,加热,就可以完成高温下“Fe与水蒸气反应的实验”。
请回答下列问题:
(1)写出反应的化学方程式: 。
(2)实验开始时,应先点燃 (填写“酒精灯”或“酒精喷灯”),。
(3)干燥管中盛装的物质可以是 (填写一种即可),检验气体A的方法:
。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年内蒙古巴彦淖尔市中学巴市一中高一上学期12月月考化学试卷 题型:实验题
(8分)铁不能与冷、热水反应,但能与水蒸气反应。如下图所示,在装置的硬质玻璃管内放入还原铁粉和石棉绒的混合物,通入水蒸气,加热,就可以完成高温下“Fe与水蒸气反应的实验”。
请回答下列问题:
(1)写出反应的化学方程式: 。
(2)实验开始时,应先点燃 (填写“酒精灯”或“酒精喷灯”),。
(3)干燥管中盛装的物质可以是 (填写一种即可),检验气体A的方法:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com