
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= __________,已知:K3000C>K3500C,则该反应是______热反应。
(2)图中表示NO2的变化的曲线是_____________;用O2表示从0~2 s内该反应的平均速率v=____________
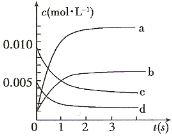
(3)能说明该反应已达到平衡状态的是____________ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是____________
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(5)关于该反应的下列说法中,正确的是________(填字母)。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
【答案】K= c2(NO2) / c2(NO)﹒c(O2) 放热 b 1.5×10-3mol·L-1·s-1 bc c D
【解析】
(1)该反应的平衡常数表达式:K= c2(NO2) / [c2(NO)﹒c(O2)]
答案为:c2(NO2) / [c2(NO)﹒c(O2)]
已知:K3000C>K3500C,说明升高温度平衡逆向移动,所以正反应为放热反应。答案:放热
(2)从反应方程式可以看出,一氧化氮和二氧化氮的变化量应该相等。根据表中数据和图像起点可知,一氧化氮的变化曲线为c,所以图中表示NO2变化的曲线是b。答案为b
用O2表示从0~2 s内该反应的平均速率v=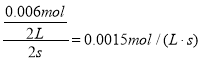
答案为1.5×10-3mol·L-1·s-1
(3)a.v(NO2)=2v(O2),不管反应进行到什么程度(反应达平衡前),此关系均成立,不一定是平衡状态;
b.因为反应前后气体的分子数不等,所以当容器内压强保持不变时,反应达平衡状态;
c.v逆(NO)=2v正(O2),此关系表明反应进行的方向相反,且数值之比等于化学计量数之比,反应达平衡状态;
d.因为气体的总质量不变,气体的体积不变,所以容器内气体的密度始终保持不变,反应不一定达平衡状态。
故答案为bc
(4)a.及时分离除NO2气体,平衡正向移动,但反应速率减慢,不合题意;
b.适当升高温度,反应速率加快,但平衡逆向移动,不合题意;
c.增大O2的浓度,反应速率加快,平衡正向移动,符合题意;
d.选择高效催化剂,反应速率加快,平衡不移动,不合题意。
答案为c
(5)该反应为体积缩小的放热反应,所以ΔH<0,ΔS<0。
答案为D。


科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 铅蓄电池的正极反应为PbO2+4H++2e-===Pb2++2H2O
B. 以CO和O2构成的碱性燃料电池负极电极反应式为CO+4OH--2e-===CO![]() +2H2O
+2H2O
C. 电解法精炼铜时,以粗铜作阴极,纯铜作阳极
D. 工业上通过电解氯化钠溶液制备金属钠和氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,某种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用较长时间。下图是一个电化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH![]() 2K2CO3+6H2O。
2K2CO3+6H2O。
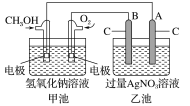
请填空:
(1)充电时,①燃料电池的负极与电源________极相连。
②阳极的电极反应式为:________________________。
(2)放电时:负极的电极反应式为:__________________。
(3)在此过程中若完全反应,乙池中A极的质量增加648 g,则甲池中理论上消耗O2____________L(标准状况)。
(4)若在常温常压下,1 g CH3OH燃料生成CO2和液态H2O时放热22.68 kJ,表示该反应的热化学方程式为:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )
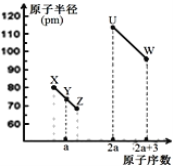
A.U、X、W三种元素最高价含氧酸酸性依次增强
B.由Y、Z和氢三种元素形成的化合物中一定只含共价键
C.XZ2与X60的化学键类型和晶体类型都相同
D.1molU的氧化物中含4NA个共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Na+、NH4+、Ca2+、Cl–、SO42–、CO32–中的若干种。为了确定该溶液的组成,进行如下实验:
①取100 mL上述溶液,加入足量氯化钡溶液,充分反应后将沉淀过滤、洗涤、干燥,得到4.30 g固体。向该固体中加过量的稀硝酸,仍有2.33 g固体未溶解。
②向①的滤液中加入足量NaOH,加热,产生使湿润的红色石蕊试纸变蓝的气体0.448 L(气体全部逸出,且已经换算成标准状况下体积)。以下说法正确的是
A.原溶液中SO42–、CO32–和NH4+一定存在,Cl-一定不存在
B.原溶液中一定不存在Ca2+,无法判断Na+是否存在
C.原溶液中可能存在Cl-,且c(Na+) ≥ 0.200 mol· L-1
D.为确定原溶液中Cl-是否存在,可以取实验①的滤液,加硝酸酸化的AgNO3进行检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请写出指定物质对应的化学式。消毒剂碘伏中含有碘分子_____________,胶卷中必不可少的感光材料_____________,加碘盐中含有碘酸钾_____________,发酵粉含有小苏打_____________。
(2)化工厂镁着火,不能用二氧化碳灭火,用化学方程式解释__________________________。
(3)电解饱和食盐水是氯碱工业的基础,写出化学方程式__________________________。
(4)稀醋酸处理热水瓶中水垢(主要成分为碳酸钙)的离子方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+Cl2(g)=2HCl(g) ΔH= -184.6kJ/mol,则![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g)的ΔH为( )
Cl2(g)=HCl(g)的ΔH为( )
A.+184.6kJ/molB.-92.3kJ/molC.-369.2kJ/molD.+92.3kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定乙醇分子(C2H6O)中活泼氢原子个数,采用下列装置,通过测定乙醇与金属钠反应放出氢气的多少进行计算。
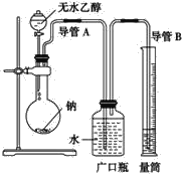
(1)指出实验装置中的错误:__。
(2)若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得氢气的体积将__(填“偏大”、“偏小”或“不变”)。
(3)请指出能使实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色) ![]() 2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
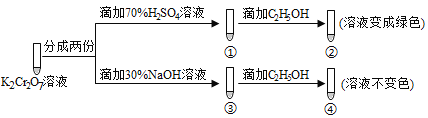
A. ①中溶液橙色加深,③中溶液变黄 B. ②中Cr2O72-被C2H5OH还原
C. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 D. 对比②和④可知K2Cr2O7酸性溶液氧化性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com