
| A. | X最高价氧化物对应的水化物为强酸 | |
| B. | 原子半径大小顺序为M>W>X>Y>Z | |
| C. | 水溶液中Z 的简单单核离子能促进水的电离 | |
| D. | Z、M的最高价氧化物对应的水化物均能溶解W与X形成的化合物 |
分析 X、Y、Z、W、M五种短周期元素,Y形成化合物种类最多,则Y为C元素;M为短周期主族元素中原子半径最大的元素,则M为Na;X2-、W3+具有相同的电子层结构,X、Y同周期,则X为O元素、W为Al;Z、W处于同一周期,X、Y 原子最外层电子数之和(6+4)等于Z、W 原子最外层电子数之和,则Z的最外层电子为10-3=7,则Z为Cl,据此解答.
解答 解:X、Y、Z、W、M五种短周期元素,Y形成化合物种类最多,则Y为C元素;M为短周期主族元素中原子半径最大的元素,则M为Na;X2-、W3+具有相同的电子层结构,X、Y同周期,则X为O元素、W为Al;Z、W处于同一周期,X、Y 原子最外层电子数之和(6+4)等于Z、W 原子最外层电子数之和,Z的最外层电子为10-3=7,则Z为Cl,
A.X是氧,无最高价氧化物,故A错误;
B.同周期自左而右原子半径减小,一般电子层越多原子半径越大,故原子半径:M(Na)>W(Al)>Z(Cl)>Y(C)>X(O),故B错误;
C.水溶液中Z的简单单核离子氯离子不能促进水的电离,故C错误;
D.W与X形成的化合物为Al2O3,是两性氧化物,能溶于强酸HClO4和强碱NaOH,故D正确;
故选:D.
点评 本题考查位置结构性质的关系和应用,推断元素是解题关键,注意对元素周期律的理解掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
| A. | 反应在前2 s 的平均速率v(O2)=0.4 mol•L-1•s-1 | |
| B. | 保持其他条件不变,体积压缩到1.0 L,平衡常数将增大 | |
| C. | 相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率大于10% | |
| D. | 保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z | M |
| A | Fe | FeCl2 | FeCl3 | Cl2 |
| B | C | CO | CO2 | O2 |
| C | CO2 | Na2CO3 | NaHCO3 | NaOH |
| D | AlO2- | Al(OH)3 | Al3+ | CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X(括号中的物质为杂质) | ① | ② |
| A | 乙酸乙酯(乙醇) | 饱和碳酸钠溶液 | 萃取、分液 |
| B | BaSO4(BaSO3) | 稀硝酸 | 过滤 |
| C | NaCl(Na2CO3) | 盐酸 | 蒸发结晶 |
| D | 铜(铝) | 浓硫酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红宝石、玛瑙、水晶、钻石等装饰品的主要成分都不相同 | |
| B. | 将Al2(SO4)3溶液蒸干、灼烧至恒重,最终剩余固体是Al2O3 | |
| C. | 白磷、臭氧、碳-60、氩、水等物质都是由分子构成的,分子内都存在共价键 | |
| D. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
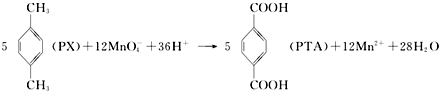
| A. | PTA是该反应的氧化产物 | |
| B. | PTA与乙二醇通过加聚反应即可生产PET塑料 | |
| C. | PX分子含有苯环的同分异构体还有3种 | |
| D. | 该反应消耗1molPX,共转移10mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 装置 | 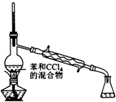 | 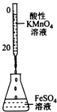 | 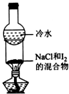 | 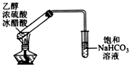 |
| 实验目的 | 分离苯和CCl4 | 酸性KmnO4溶液滴定FeSO4溶液 | 除去NaCl中的I2 | 制备和收集少量乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- | |
| B. | 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| D. | Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-═2Fe2++I2+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
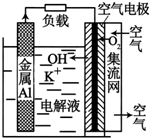 铝-空气电池以高纯度铝(含铝99.99%)为负极,氧气为正极,以KOH溶液为电解质溶液.如图为某铝-空气电池工作的原理示意图,下列有关说法正确的是( )
铝-空气电池以高纯度铝(含铝99.99%)为负极,氧气为正极,以KOH溶液为电解质溶液.如图为某铝-空气电池工作的原理示意图,下列有关说法正确的是( )| A. | 铝-空气电池要及时回收处理,以免造成重金属污染 | |
| B. | 每消耗1molAl,电解质溶液中会有3 mol电子通过 | |
| C. | 负极上的电极反应式为:Al-3e-+4OH-═AlO2-+2H2O | |
| D. | 电池总反应式为:Al+KOH+O2═KAlO2+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com