
分析 (1)NaCN 喷淋了H2O2 溶液使NaCN转化为无毒的NaHCO3和NH3,结合反应物与生成物书写反应;
(2)C元素的化合价由+2价升高为+4价,双氧水中O元素的化合价降低;
(3)n(NH3)=$\frac{4.48L}{22.4L/mol}$=0.2mol,结合C元素的化合价计算转移电子;
(4)反应后固体MnO2质量不变,作催化剂,可知过氧化氢分解生成水和氧气.
解答 解:(1)NaCN 喷淋了H2O2 溶液使NaCN转化为无毒的NaHCO3和NH3,由反应物与生成物可知反应为NaCN+H2O2+H2O═NaHCO3+NH3↑,
故答案为:NaCN+H2O2+H2O═NaHCO3+NH3↑;
(2)C元素的化合价由+2价升高为+4价,双氧水中O元素的化合价降低,则被氧化的元素为C,氧化剂为H2O2,故答案为:C;H2O2;
(3)n(NH3)=$\frac{4.48L}{22.4L/mol}$=0.2mol,由反应可知0.2molNaCN失去电子,由C元素的化合价变化可知转移电子为0.2mol×(4-2)=0.4mol,故答案为:0.4;
(4)①反应后固体MnO2质量不变,作催化剂,故答案为:催化剂;
②可知过氧化氢分解生成水和氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素分析仪可以确定物质中是否含有C、H、O、N、Cl、Br等元素 | |
| B. | 用红外光谱仪可以确定物质中是否存在某些有机原子团 | |
| C. | 用原子吸收光谱可以确定物质中含有哪些金属元素 | |
| D. | 焰色反应适用于所有金属元素的鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青蒿素是含有三种元素的有机化合物 | |
| B. | 青蒿素分子中C、H、O原子个数比为15:22:5 | |
| C. | 从黄花蒿提取青蒿素发生了化学变化 | |
| D. | 提取过程中用到了萃取原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH固体置于大小相同的滤纸上称量 | |
| B. | 蒸馏操作时,冷凝水的方向须与气体的流向相同 | |
| C. | 配制稀硫酸时,将浓硫酸溶解后直接转移入容量瓶 | |
| D. | 分液时,先要打开分液漏斗上口活塞,再打开旋塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
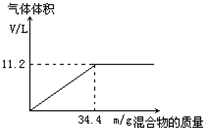 在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热充分反应.如图表示加入的混合物的质量与产生的气体体积(标准状况)的关系.
在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热充分反应.如图表示加入的混合物的质量与产生的气体体积(标准状况)的关系.查看答案和解析>>
科目:高中化学 来源: 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com