

分析 (1)反应热与物质的聚集状态有关,聚集状态不同,反应热不同;
(2)ⅰ.计算平衡时氢气、水的浓度,再根据K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$计算平衡常数;
保持温度不变,向该密闭容器中再充入1mol CO2(g)和1mol H2O(g),相当于增大压强,增压平衡向气体系数小的方向移动;
ⅱ.平衡时满足V正=V逆,v正=k正•c(A)a•c(B)b;V逆=k逆•c(C)c•c(D)d,则k逆:k正=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$=K;
(3)①根据三行式计算得到;
②根据图示信息:X轴上a点的数值比b点小,随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,结合平衡移动原理回答.
解答 解:(1)反应热与物质的聚集状态有关,聚集状态不同,反应热不同,上述反应与氢气燃烧热的反应中水的状态不同,所以不能求出上述反应的焓变;
故答案为:不能;因为上述反应与氢气燃烧热的反应中水的状态不同;
(2)ⅰ平衡时甲醇为0.75mol/L、二氧化碳为0.25mol/L,则:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始浓度(mol/L):1 3 0 0
变化浓度(mol/L):0.75 2.25 0.75 0.75
平衡浓度(mol/L):0.50 0.75 0.75 0.75
则平衡常数K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$=$\frac{0.75×0.75}{0.25×0.7{5}^{2}}$=$\frac{16}{3}$=5.33;
保持温度不变,向该密闭容器中再充入1mol CO2(g)和1mol H2O(g),相当于增大压强,增压平衡向气体系数小的方向移动,即向正方向移动;
故答案为:5.33;正向;
ⅱ平衡时满足V正=V逆,v正=k正•c(A)a•c(B)b;V逆=k逆•c(C)c•c(D)d,
则k逆:k正=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$=K=3:16;
故答案为:3:16;
(3)①设CO的转化量是x,则
CO(g)+2H2(g)?CH3OH(g);
初始量:1mol 2mol 0
变化量:x 2x x
平衡量:1-x 2-2x x
平衡时,CH3OH的体积分数为10%,则$\frac{x}{1-x+2-2x+x}$×100%=10%,x=0.25,所以CO的转化率为$\frac{0.25mol}{1mol}$×100%=25%,故答案为:25%;
②根据图示信息:X轴上a点的数值比b点小,随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,平衡逆向移动,故Y表示温度,故答案为:小;温度;随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,平衡逆向移动,故Y表示温度.
点评 本题为综合题,涉及反应热的计算、化学平衡平衡移动影响因素、化学平衡常数计算、平衡移动原理的应用,题目难度中等,明确化学平衡常数的概念及表达式为解答关键,本题也可以利用三段式计算,试题培养了学生的分析能力及化学计算能力.


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:选择题
| A. | 水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物 | |
| B. | 下雪后,常用播撒NaCl颗粒方法来防止道路结冰 | |
| C. | 用活性炭为糖浆脱色和用SO2漂白纸浆的原理不同 | |
| D. | 在医学上用BaSO4做钡餐,是因为Ba2+对人体无毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
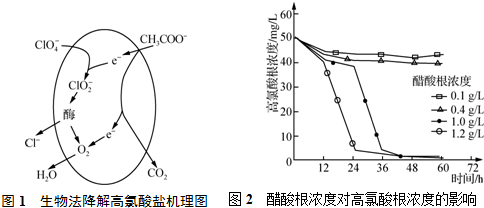
| 酸 | HClO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 1.6×10-9 | 4.2×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | △H(kJ•mol-1) | 平衡常数(K) |
| 4NH3 (g)+5O2 (g)?4NO (g)+6H2O (g) | -905.5 | 1.1×1026mol•L-1 |
| 4NH3 (g)+4O2 (g)?2N2O (g)+6H2O (g) | -1104.9 | 4.4×1028 |
| 4NH3 (g)+3O2 (g)?2N2 (g)+6H2O (g) | -1269.0 | 7.1×1034L•mol-1 |

| 沉淀物 | Ksp |
| FeCO3 | 3.0×10-11 |
| MnCO3 | 2.0×10-11 |
| NiCO3 | 1.0×10-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
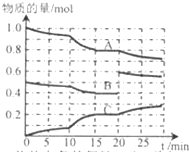 在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:
在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向纯水中投入一小块金属钠 | B. | 将水加热煮沸 | ||
| C. | 向水中通入SO2 | D. | 向水中加入NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol H2O中所含的粒子数目一定是NA | |
| B. | 1 molNH4+所含的质子数是10NA | |
| C. | 51 g NH3所含原子数为3NA | |
| D. | 氧气的相对分子质量与2NA个氧原子质量(以g为单位)在数值上相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com