
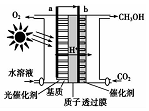
 科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )
科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )| A. | 该新型电池仅存在化学能与电能的转化 | |
| B. | 电池总反应为2CO2+4H2O=2CH3OH+3O2 | |
| C. | 电子从电极b流向电极a | |
| D. | 产生标准状况下2.24 LO2,转移电子0.6NA |
分析 由示意图可知a电极水中氢氧根失电子放出氧气为负极,电极反应式为2H2O-4e-=4H++O2,b电极二氧化碳得电子结合氢离子生成甲醇为正极,电极反应式为CO2+6H++6e-=CH3OH+H2O,电池总反应为2CO2+4H2O=2CH3OH+3O2,电子从负极流向正极,据此解答该题.
解答 解:A、由示意图可知,该新型电池仅存在、太阳能、化学能与电能的转化,故A错误;
B、根据以上分析,电池总反应为2CO2+4H2O=2CH3OH+3O2,故B正确;
C.电子从负极a流向正极b,故C错误;
D.负极,电极反应式为2H2O-4e-=4H++O2,则产生标准状况下2.24 LO2,转移电子0.4NA,故D错误;
故选B.
点评 本题考查原电池知识,题目难度中等,本题注意把握电极方程式的方法.


科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物对应水化物的酸性:W>X | |
| B. | X、Y的单质均具有较高的熔沸点 | |
| C. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| D. | Z、W形成的化合物中既含有离子键,又含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C2H4O2的有机物不一定是乙酸 | |
| B. | 乙炔与足量Br2发生加成反应生成1,1,2,2-四溴乙烷 | |
| C. | 淀粉、蔗糖、葡萄糖在一定条件下都能发生水解反应 | |
| D. | 实验室用乙醇和浓H2SO4制备乙烯时,反应液体的温度要迅速上升到170℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | 除②、③、⑥外 | C. | 除②、④、⑦外 | D. | 除③、⑥、⑦外 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0×10-7mol•L-1 | B. | 1.0×10-6mol•L-1 | ||
| C. | 1.0×10-2mol•L-1 | D. | 1.0×10-12mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L Na2CO3和NaHCO3的溶液中:二者的PH不同,但溶液中粒子种类相同 | |
| B. | pH=5的CH3COOH溶液和PH=5的NH4Cl溶液中,c(H+)前者大于后者 | |
| C. | 在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降,Ksp(Ag2S)减小 | |
| D. | Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaH在水中显酸性 | |
| B. | NaH中氢离子电子排布与氦原子相同 | |
| C. | NaH中氢离子半径比锂离子的大 | |
| D. | NaH中氢离子可以被还原成氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com