
���ĸ������ͬ���ܱ������зֱ����һ������SO2��O2����ʼ��Ӧʱ��������Ӧ�����ɴ�С˳��������ȷ���ǣ���
�ף���500��ʱ��SO2��O2��10mol��Ӧ
�ң���500��ʱ����V2O5��������10mol SO2��5mol O2��Ӧ
������450��ʱ��8mol SO2��5mol O2��Ӧ
������500��ʱ��8mol SO2��5mol O2��Ӧ��
A�� �ס��ҡ������� B�� �ҡ��ס������� C�� �ҡ��ס������� D�� ���������ҡ���
���㣺 ��Ӧ���ʵĶ�����ʾ������
ר�⣺ ��ѧ��Ӧ����ר�⣮
������ ������������Է�Ӧ���ʵ�Ӱ�죬�ÿ��Ʊ������жϷ�Ӧ������Դ�С��Ȼ������ע������Է�Ӧ���ʵ�Ӱ�����
��� �⣺��������ȣ�SO2Ũ����ȣ�����������Ũ�ȴ�����ʹ�ô���������������ͬ�����ڶ��������Ũ��һ��������Ũ�ȵ�Ӱ�첻�����Ӱ���ʹ�ô�����Ӧ���ʸ��죬���Է�Ӧ���ʣ��ң��ף�
���붡��ȣ�����SO2��O2�����ʵ����ȶ��д�SO2��O2��Ũ�ȱȶ��д�����������ͬ��Ũ��Խ��Ӧ����Խ�죬���Է�Ӧ���ʣ��ף�����
���붡��ȣ�����������ͬ�������¶ȸߣ��¶�Խ�ߣ���Ӧ����Խ�죬���Է�Ӧ���ʣ���������
�����ɴ�С��˳�������ҡ��ס���������
��ѡC��
������ ���⿼�黯ѧ��Ӧ���ʵ�Ӱ�����أ��ѶȽ�С�����ÿ��Ʊ�����̽��������ضԷ�Ӧ����Ӱ�죮


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ʾװ���У��۲쵽������ָ��ƫת��M����֣�N����ϸ���ɴ��ж��±�������M��N��P���ʣ����п��Գ������ǣ���
M N P
A п ͭ ϡ������Һ
B ͭ �� ϡ����
C �� п ��������Һ
D п �� ��������Һ
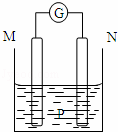
A�� A B�� B C�� C D�� D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и����Ȼ�ѧ����ʽ�У���ѧ��Ӧ�ġ�Hǰ�� ���ں��ߵ��ǣ���
���ں��ߵ��ǣ���
��C��s��+O2��g��═CO2��g������H1 C��s��+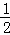 O2��g��═CO��g������H2
O2��g��═CO��g������H2
��S��s��+O2��g��═SO2��g������H3 S��g��+O2��g��═SO2��g������H4
��H2��g��+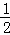 O2��g��═H2O��l������H5 2H2��g��+O2��g��═2H2O��l������H6
O2��g��═H2O��l������H5 2H2��g��+O2��g��═2H2O��l������H6
��CaCO3��s��═CaO��s��+CO2��g������H7 CaO��s��+H2O��l��═Ca��OH��2��s������H8��
A�� �� B�� �� C�� �ڢۢ� D�� �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������3���Ȼ�ѧ����ʽ��
2H2S��g��+3O2��g��=2SO2��g��+2H2O��l����H=﹣Q1 kJ/mol
2H2S��g��+O2��g��=2S��s��+2H2O��l����H=﹣Q2 kJ/mol
2H2S��g��+O2��g��=2S��s��+2H2O��g����H=﹣Q3 kJ/mol
�ж�Q1��Q2��Q3���߹�ϵ��ȷ���ǣ���
A�� Q1��Q2��Q3 B�� Q1��Q3��Q2 C�� Q3��Q2��Q1 D�� Q2��Q1��Q3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������Է�ĩ״���ڣ��Ͱ�������������ͬ�������壮��֪��
��Sn��s���ף�+2HCl��aq��═SnCl2��aq��+H2��g����H1
��Sn��s���ң�+2HCl��aq��═SnCl2��aq��+H2��g����H2
��Sn��s���ң�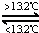 Sn��s���ף���H3=+2.1kJ•mol﹣1��
Sn��s���ף���H3=+2.1kJ•mol﹣1��
����˵����ȷ���ǣ���
A�� ��H1����H2
B�� ���ڳ������Ի���״̬����
C�� ����תΪ�����ķ�Ӧ�Ƿ��ȷ�Ӧ
D�� ���������ڴ��ڵ���13.2��Ļ����У������лٻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ������̫���ֽܷ�ˮ���ɵ������ڴ�����������CO2��Ӧ���ɼ״���CH3OH������������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�أ���֪H2��g����CO��g����CH3OH��l����ȼ���ȡ�H�ֱ�Ϊ﹣285.8kJ/mol��﹣283.0kJ/mol��﹣726.5kJ/mol����ش��������⣺
��1����̫���ֽܷ�5molˮ���ĵ������� kJ��
��2���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽΪ ��
��3����֪25�桢101kPa�£�H2O��l��═H2O��g����H=+44kJ•mol﹣1����1g�״���CH3OH��ȼ�� ����CO2����̬ˮʱ�ų�������Ϊ ��
����CO2����̬ˮʱ�ų�������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ö��Ե缫���������Һ��һ��ʱ����ټ���һ����������һ�����ʣ������ڣ�����Һ����ԭ����Һ��ȫһ�����ǣ���
A�� CuCl2��CuO�� B�� NaCl��HCl�� C�� NaOH��NaOH�� D�� CuSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ŀǰ����ѧ�������о�����һ�ָ��ܵ��﹣﹣�����أ����������ơ���Ϊ�������Ե���Ħ�﹣A2lO3�մ����������ʣ���Ӧʽ���£�Na2SX 2Na+xS����˵����ȷ���ǣ���
2Na+xS����˵����ȷ���ǣ���
A�� �ŵ�ʱ��Na��������S��������ԭ��Ӧ
B�� �ŵ�ʱ��Na������ԭ��Ӧ
C�� ���ʱ���� �������Դ����������
�������Դ����������
D�� ���ʱ�����������ķ�ӦΪ��SX2﹣﹣2e=xS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������������ġ���ɫ��ѧ����ָ��ѧ��ҵ�����У���
A�� �Է�ˮ�����������������ϸ���
B�� ���ŷ��κ��к�����
C�� �ڻ���������Χ�ֲݡ��������ֻ���ʹ������Ϊ��ʽ����
D�� ����ɫֲ��Ϊԭ�ϣ����������ʵ�ֻ����������̵Ļ�ѧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com