
| A、只有①?? |
| B、只有①②?? |
| C、只有①②③?? |
| D、全部 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
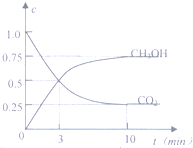 目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的客闭容器中,充入1molCO2和3molH2,在500℃下发生反应:CO2(g)+3H2O(g)?CH3OH(g)+H2O(g);
目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的客闭容器中,充入1molCO2和3molH2,在500℃下发生反应:CO2(g)+3H2O(g)?CH3OH(g)+H2O(g);查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KHCO3 KAlO2 K2CO3 KCl |
| B、K2CO3 KOH KHCO3 KCl |
| C、K2SO4 KOH KHSO4 KCl |
| D、K2CO3 K2SiO3 KOH KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强度高 | B、不易生锈 |
| C、密度小 | D、导电、导热性好 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO32-、Na+、K+、OH- |
| B、Ba2+、CO32-、NO3-、SO42- |
| C、K+、Cu2+、Cl-、SO42- |
| D、Fe2+、NO3-、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③⑤ | B、只有①②③ |
| C、只有①②③④ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锌片是正极,铜片质量不变 |
| B、电流方向是从锌片流向铜片 |
| C、锌片是负极,铜片质量不变 |
| D、锌片是负极,铜片质量增加 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com