
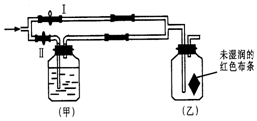
 如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,再通入乙瓶,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色.甲瓶中所盛的试剂可能是( )
如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,再通入乙瓶,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色.甲瓶中所盛的试剂可能是( ) | A. | ① | B. | ②③④ | C. | ①③④ | D. | ③④ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | NaHCO3是碱 | B. | NaHCO3是酸 | C. | NaHCO3是盐 | D. | NaHCO3是一元酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2[SO42-]=[NH4+]>[H+]=[OH-] | B. | [SO42-]>[NH4+]]>[H+]=[OH-] | ||
| C. | [NH4+]]>[SO42-]>c(OH-)>c(H+) | D. | [NH4+]]>[SO42-]>[H+]>[OH-] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可能存在NaCl | B. | 可能存在Na2SO4 | C. | 一定存在FeCl3 | D. | 一定存在Ba(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 品名 | 浓缩菠萝汁 |
| 配料 | 水、浓缩菠萝汁、蔗糖、柠檬酸、甜蜜素、维生素C、菠萝香精、 柠檬黄、日落黄、山梨酸钾等 |
| 果汁含量 | ≥80%生产日期标于包装袋封口上 |
| 实例 | 性质 |
| 紫外线消毒 | 变性 |
| 蛋白质遇浓硝酸变黄 | |
| 误食了重金属离子,可以立即喝大量的牛奶来缓解 毒性 | |
| 鸡蛋清溶液中加入少量饱和的硫酸铵溶液出现沉淀 | |
| 常用酒精清洗伤口 | |
| 蒸煮鸡蛋食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
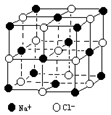 晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl晶体结构如图所示.
晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl晶体结构如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向浓氢氧化钠溶液中通入少量的CO2气体:CO2+OH-═HCO3- | |
| B. | 过量的NaHSO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 澄清石灰水中滴加少量的小苏打溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| D. | 向Na2S2O3溶液中通入过量的氯气:S2O32-+2Cl-+3H2O═2SO32-+4Cl-+6H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
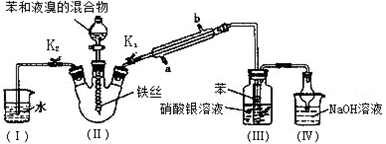
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com