
下列关于电离平衡常数(K)的说法正确的是
A.不同浓度的同一弱电解质,其电离平衡常数(K)不同
B.电离平衡常数(K)越小,表示弱电解质电离能力越弱
C.多元弱酸各步电离平衡常数相互关系为:K1<K2<K3
D.CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小
 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在元素
周期表中相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
A.X的最常见气态氢化物的水溶液显酸性
B.最高价氧化物对应水化物的酸性W比Z强
C.Z的单质与氢气反应较W剧烈
D.X的原子半径小于Y
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁、戊五种短周期元素原子序数依次递增。甲最
外层电子数是次外层的两倍,丙的次外层电子数比最外层少4个,丁形成的简单阳离子是同周期元素简单
离子中半径最小的,戊是同周期主族元素中原子半径最小的。试用化 学式回答下列问题:
学式回答下列问题:
(1)乙和戊形成的化合物中各原子最外层均满足8e-结构,其化学式为 ;
(2)写出乙的最高价氧化物的水化物的浓溶液与甲单质反应的化学方程式
;
(3)戊的最高价氧化物与丁的最高价氧化物的水化物反应的离子反应方程式为
;
(4) 常温下戊单质被NaOH溶液吸收的化学方程式为 ;
(5)氢与丙形成原子个数比为1:1的液体,该物质中存在的作用力有( )
①极性键 ②非极性键 ③离子键 ④氢键 ⑤范德华力
④氢键 ⑤范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W在周期表中的相对位置如图,W
原子的最外层电子数是其最内层电子数的3倍。下列判断正确的是
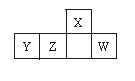 A.原子半径:X>Y>Z>W
A.原子半径:X>Y>Z>W
B.含Y元素的盐溶液有的显酸性,有的显碱性
C.最简单气态氢化物的热稳定性:Z >W
D.X的氢化物能与其最高价氧化物对应的水化物反应生成盐
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学反应速率的认识正确的是
A.H+和OH—的反应活化能接近于零,反应几乎在瞬间完成
B.对于任何化学反应来说,反应速率越大,反应现象就越明显
C.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大
D.化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,将一定量的冰醋酸(无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示。

请完成下列问题:
(1)上述a、b、c三点对应醋酸的电离程度最大的是 (填“a”、“b”、“c”),三点对应溶液中c(OH-)由大到小的顺序为 。
(2)c点对应的溶液中c(H+)与c(CH3COO-)+c(OH-)的关系为前者 (填“大于”“小于”“等于”)后者。
(3)从a点到b点,溶液中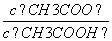 的比值 (填“增大”、“减小”、“等于”)。
的比值 (填“增大”、“减小”、“等于”)。
(4)25 ℃时,体积均为100 mL 、pH=m的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示。则稀释前两溶液中c(OH-)= , HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。

(5)若用pH试纸进行实验,你能否区分上述HX和CH3COOH两种酸溶液?若能,请简述操作过程;若不能,请说明理由。 。
查看答案和解析>>
科目:高中化学 来源: 题型:
上图为元素周期表截取的短周期的一部分,即 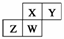 。 四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )
。 四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )
A.原子半径:W>Z>Y>X
B.气态氢化物 的稳定性:Z>W>X>Y
的稳定性:Z>W>X>Y
C.W的最高正化合价与负化合价的绝对值可能相等
D.Z的最高价氧化物的水化物可能为强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组借助右图装置完成收集NO气体的实验。
正确的操作是( )
A.从①口进气,用排水法集气
B.从①口进气,用排气法集气
C.从②口进气,用排水法集气
D.从②口进气,用排气法集气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com