
分析 氧化还原反应中化合价升降一定相等,该反应中氯气为氧化剂,碘单质为还原剂,根据化合价变化列式计算氧化剂与还原剂的物质的量之比.
解答 解:反应Cl2+I2+H2O→HIO3+HCl中,Cl2中氯原子从而0价变为-1价被还原,Cl2为氧化剂,1mol氯气反应化合价降低2mol;
I2的化合价从0价变为HIO3中的+5价,化合价升高5价,HIO3为还原剂,1mol碘单质完全反应化合价升高5×1mol×2=10mol,
氧化还原反应中化合价升降相等,设氯气的物质的量为x、碘单质的物质的量为y,则2x=10y,整理可得:x:y=5:1,
所以该反应中氧化剂与还原剂的物质的量之比为5:1,
故答案为:5:1.
点评 本题考查了氧化还原反应,题目难度不大,明确氧化还原反应的特征为解答关键,注意掌握配平氧化还原反应的方法,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+的结构示意图为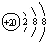 | B. | CO2分子的比例模型示意图: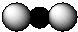 | ||
| C. | 水合钠离子: | D. | 次氯酸的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
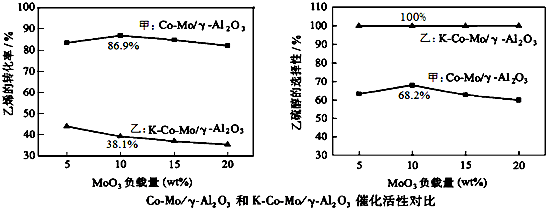
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 添加A物质 | B. | 升高体系温度 | C. | 及时分离出C物质 | D. | 减少B物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| B. | 硫酸铜溶液显酸性:Cu2++2H2O=Cu(OH)2↓+2H+ | |
| C. | 向碳酸氢铵溶液中加过量澄清石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| D. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com