
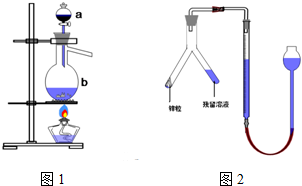
分析 (1)由仪器的结构可知,a为分液漏斗,b为蒸馏烧瓶;液体加热需要防止暴沸;氯水具有漂白性,是由于HClO的强氧化性;
(2)仪器b中二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气与水;
(3)检验装置气密性后,向烧瓶中加入二氧化锰,再从分液漏斗中加入盐酸,最后加热制备氯气;
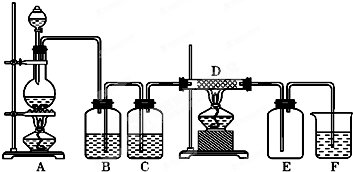
(4)若残留溶液转移到锌粒中,Y形管内壁会残留溶液,HCl不能与Zn完全反应;
读取体积时要满足压强回复到原压强,而且眼的视线要与液体的凹液面相切;
甲同学的方案:二氧化锰与浓盐酸反应生成氯化锰,也会与硝酸银反应,实验不可行.
解答 解:(1)由仪器的结构可知,a为分液漏斗,b为蒸馏烧瓶;b中加入碎瓷片的作用是:防止暴沸;氯水具有漂白性,是由于HClO的强氧化性,
故答案为:分液漏斗;蒸馏烧瓶;防止暴沸;HClO;
(2)仪器b中二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气与水,反应离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑;
(3)检验装置气密性后,向烧瓶中加入二氧化锰,再从分液漏斗中加入盐酸,最后加热制备氯气,
故答案为:A、C、D;
(4)若残留溶液转移到锌粒中,Y形管内壁会残留溶液,HCl不能与Zn完全反应,使测得的气体的量不准确,测得的盐酸的浓度不准,因此应将锌粒转移至残留溶液中,
压强对气体的体积有影响,该反应是在加热条件下进行的,温度升高气体压强增大,如果不回复到原温度,相当于将气体压缩了,使得测出的气体的体积减小,故温度要恢复到原温度时,同时上下移动右端的漏斗,使两端的液面的高度相同,视线要与液体的凹液面相切,读取测量气体的体积,
甲同学的方案中二氧化锰与浓盐酸反应生成氯化锰,也会与硝酸银反应,实验不可行,乙同学方案可能,
故答案为:将锌粒转移至残留溶液中;恢复至室温;乙.
点评 本题考查氯气的实验室制备、物质含量测定实验等,涉及化学仪器、对操作的分析评价、对实验原理的分析评价等,是化学实验综合考查,难度中等.


 培优口算题卡系列答案
培优口算题卡系列答案科目:高中化学 来源: 题型:解答题
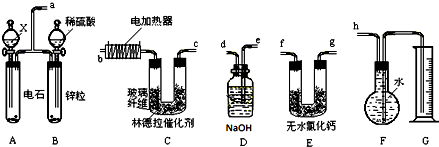
 如图所示,A是氯气的发生装置,B、C是净化气体的装置,D中装铁丝网;反应后E的底部有棕色固体聚集;F是吸收多余气体的装置.
如图所示,A是氯气的发生装置,B、C是净化气体的装置,D中装铁丝网;反应后E的底部有棕色固体聚集;F是吸收多余气体的装置.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示的装置为铁的吸氧腐蚀实验.一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,可观察到现象为铁钉附近的溶液有蓝色沉淀,该反应的离子方程式为Fe2++[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓; 向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为O2+4e-+2H2O=4OH.
如图所示的装置为铁的吸氧腐蚀实验.一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,可观察到现象为铁钉附近的溶液有蓝色沉淀,该反应的离子方程式为Fe2++[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓; 向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为O2+4e-+2H2O=4OH.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
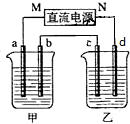 如图所示装置中,甲、乙两个烧杯分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙两个烧杯分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液,电极均为石墨电极.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
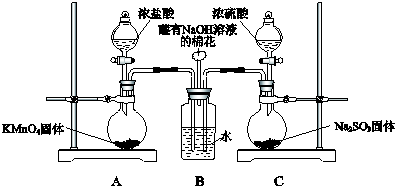
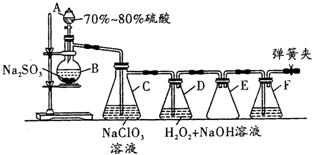 用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用如图所示装置(部分支持装置省略)制备少量的亚氯酸钠.
用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用如图所示装置(部分支持装置省略)制备少量的亚氯酸钠.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com