
| A、晶体硅是高科技的支柱材料,可用于制备太阳能电池板和光导纤维 | B、用浸泡过高锰酸钾溶液的硅藻土吸收水果产生的乙烯可以延长水果的保存期 | C、绿色化学的核心是利用化学原理对环境污染进行治理 | D、明矾常用作净水剂,目的是除去水中的悬浮杂质和有害细菌 |


科目:高中化学 来源: 题型:
| A、分子中所有原子在同一平面 | B、与氯化氢加成只生成一种产物 | C、能使酸性KMnO4溶液褪色 | D、能与溴水发生取代反应而使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它是由Te、Zn、Cd按一定比例混合而成的,无固定的溶沸点 | B、它易导电、导热,具有延展性 | C、它的熔、沸点比Zn的高 | D、它的硬度和强度比Cd的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用纯碱做治疗胃酸过多的药品 | B、SiO2是制备光导纤维的主要材料 | C、用浸泡过高锰酸钾溶液的硅藻土吸收水果产生的乙烯,以延长保质期 | D、民间用明矾作净水剂除去水中的悬浮物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铁溶液中加入还原性铁粉 | B、硫酸铁溶液中滴加硫氰化钾溶液 | C、碘水中滴加淀粉碘化钾溶液 | D、碳酸氢钠溶液中滴加稀盐酸 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:实验题
(16分)Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为 ;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式: 。
(2)请以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。其他限选试剂:3 mol·L-1 H2SO4、0.01 mol·L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
实验步骤 | 预期现象与结论 |
步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 |
; |
步骤2: ____________________________________ ____________________________________。 |
|
(3)利用(2)提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:取少量样品溶于水, 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:选择题
下列分离、提纯、鉴别物质的方法正确的是
A. 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液
B. 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体
C. 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
D. 用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质
查看答案和解析>>
科目:高中化学 来源:2015届广东省揭阳市高三上学期第一次阶段考试理综试卷(解析版) 题型:填空题
(16分)铜及其化合物在生产和生活实际中应用广泛。
Ⅰ.某学习小组对粗铜提纯(电解精炼)后的阳极泥(主要成分为银、金)进行如下实验。
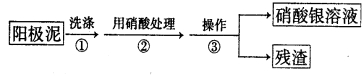
(1)操作③所需的仪器有:烧杯、 。
(2)稀硝酸处理阳极泥得到硝酸银稀溶液,写出该步反应的化学方程式_____ _。
(3)为了回收金,他们查阅了有关资料如下表:
编号 | 常温下反应 | 化学平衡常数 |
反应1 | Au + 6HNO3 | <10?5 |
反应2 | Au3+ + Cl? | >105 |
从资料中可知,常温下金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸体积比为1∶3的混合物)。请你运用化学平衡移动原理,简要说明金能溶于王水的原因: 。
Ⅱ.实验室用铜制备CuSO4溶液有多种方案,某实验小组给出了以下三种方案:
请回答有关问题:

(4)甲方案:将6.4g铜丝放到90 mL 1.5 mol·L-1的稀硫酸中,控温在50℃。加入40 mL 10%的H2O2,反应0.5小时,升温到60℃,持续反应1小时后,经一系列操作,得CuSO4·5H2O 20.0 g【已知有关摩尔质量:M(Cu)=64 g/mol, M(CuSO4·5H2O) =250 g/mol】。
①反应时温度控制在50℃~60℃,不宜过高的原因是 ;
②本实验CuSO4·5H2O的产率为 。
(5)乙方案:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质A调节pH至4 ,然后过滤、浓缩、结晶。
①物质A可选用以下的 (填序号);
A.CaO B.NaOH C.CuCO3 D.Cu2(OH)2CO3 E.Fe2(SO4)3
②反应中加入少量FeSO4可加速铜的氧化,FeSO4的作用是 ;
(6)丙方案:为了节约原料,硫酸和硝酸的物质的量之比最佳为,n(H2SO4):n(HNO3)= 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
下列有关实验正确的是
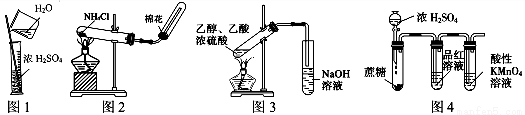
A.图1:稀释浓硫酸
B.图2:实验室制备氨气
C.图3:实验室制备乙酸乙酯
D.图4:检验浓硫酸与蔗糖反应产生的二氧化硫
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com