
| A. | 等质量的两物质分别与足量盐酸充分反应时,NaHCO3产生CO2气体多 | |
| B. | 可以用澄清石灰水或者氢氧化钠溶液区别 | |
| C. | 等质量的两物质分别与足量的等浓度盐酸反应时,一般是Na2CO3产生CO2气体快 | |
| D. | NaHCO3中Na2CO3混有杂质可以用加热方法除去 |
分析 A.等质量的Na2CO3和NaHCO3,NaHCO3物质的量较多,生成二氧化碳多,可以据此解答;
B.澄清石灰水与Na2CO3、NaHCO3均生成沉淀;
C.根据反应Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑判断;
D.NaHCO3易分解,Na2CO3难分解.
解答 解:A.等质量的Na2CO3和NaHCO3,NaHCO3物质的量较多,生成二氧化碳多,故A正确;
B.Na2CO3和NaHCO3都与澄清的石灰水反应生成沉淀,反应为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH和NaHCO3+Ca(OH)2═CaCO3↓+NaOH+H2O,所以不能用澄清石灰水区别,也不能用氢氧化钠溶液区别,故B错误;
C.由反应Na2CO3+2HCl═2NaCl+H2O+CO2↑,NaHCO3+HCl═NaCl+H2O+CO2↑可知,等质量的两物质分别与足量的等浓度盐酸反应时,NaHCO3产生CO2气体快,故C错误;
D.NaHCO3易分解,Na2CO3难分解,NaHCO3中Na2CO3混有杂质可以用加热方法不能除去,故D错误.
故选A.
点评 本题考查了Na2CO3和NaHCO3性质,题目难度不大,注意把握Na2CO3和NaHCO3性质相似点与不同点,学习中注重基础知识的积累.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
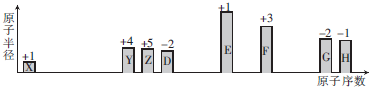
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎把浓硫酸粘在手上,立即用大量的水冲洗,涂上3%-5%的碳酸氢钠溶液 | |
| B. | 如果汽油、煤油等可燃物着火,应立即用沙土扑灭 | |
| C. | 不慎将浓碱沾到皮肤上,立即用大量的水冲洗,然后涂上硼酸溶液 | |
| D. | 酒精灯不慎碰翻着火,应立即用湿布盖灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol CH4含有的电子数为NA | |
| B. | 标准状况下,22.4L己烷中共价键数为19NA | |
| C. | 6.4g CaC2固体中所含阴离子数为0.2NA | |
| D. | 1L 1mol/L的NaHCO3溶液中含有NA个HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与铝产生氢气的溶液中:NH4+、Cl-、Mg2+、SO42- | |
| B. | 常温下PH=9的溶液中:Na+、K+、AlO2-、SO42- | |
| C. | 0.1mol/LNaOH溶液中:HCO3-、Na+、K+、Ca2+ | |
| D. | 无色溶液中:H+、Cu2+、Al3+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1MgCl2溶液 | B. | 0.1mol•L-1NH4Cl溶液 | ||
| C. | 0.1mol•L-1KCl溶液 | D. | 0.1mol•L-1 AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
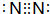 .试写出由上述元素组成的分子中含有4个原子核且为18电子结构的物质的化学式H2O2
.试写出由上述元素组成的分子中含有4个原子核且为18电子结构的物质的化学式H2O2查看答案和解析>>
科目:高中化学 来源: 题型:解答题
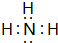 ,BA3跟C的单质在一定条件下反应,能生成化合物BC的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,BA3跟C的单质在一定条件下反应,能生成化合物BC的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=0的溶液:Fe2+、Br-、Na+、NO3- | |
| B. | 由水电离产生的c(H+)=1.0×10-12mol•L-1的溶液中:K+、AlO2-、NO3-、Na+ | |
| C. | 中性溶液中:Fe3+、K+、Al3+、SO42- | |
| D. | 在0.1 mol•L-1Na2CO3溶液中:A1O2-、Na+、NO3-、C1- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com