
| A. | 过氧化氢分解制得标准状况下1.12 L O2,转移电子数目为 0.2 NA | |
| B. | 1mol Na2CO3晶体中含CO32-离子数小于NA | |
| C. | 惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体标况下11.2L | |
| D. | 0.1mol的CaO2中含阴离子数是0.2 NA |
分析 A、用双氧水分解制取氧气,氧元素的价态由-1价变为0价;
B、碳酸钠由2个钠离子和1个碳酸根构成来分析;
C、电解饱和食盐水时,阳极上电极反应为:2Cl--2e-=Cl2;
D、CaO2由1个钙离子和1个过氧根构成.
解答 解:A、用双氧水分解制取氧气,氧元素的价态由-1价变为0价,故当生成标况下1.12L氧气即0.05mol氧气时,转移0.1NA个电子,故A错误;
B、碳酸钠由2个钠离子和1个碳酸根构成,故1mol碳酸钠中含NA个碳酸根,故B错误;
C、电解饱和食盐水时,阳极上电极反应为:2Cl--2e-=Cl2,故当电路中通过NA个电子时,生成0.5mol氯气,在标况下为11.2L,故C正确;
D、CaO2由1个钙离子和1个过氧根构成,故0.1mol过氧化钙中含0.1NA个阴离子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、纤维素、蔗糖、PVC、淀粉都是高分子化合物 | |
| B. | 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 | |
| C. | 氢键在形成蛋白质二级结构和DNA双螺旋结构中起关键作用 | |
| D. | 石油、煤、天然气、可燃冰、生物柴油都属于化石燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内消耗的A与生成的B物质的量之比为1:3 | |
| B. | 混合物各物质浓度的浓度相等 | |
| C. | 容器内A、B、C三种物质共存 | |
| D. | ν(A)、ν(B)、ν(C) 之比为1:3:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中化合价变化的有N、C元素 | |
| B. | 当x=2时,每生成1 mol N2,转移电子数为4 mol | |
| C. | 等物质的量N2和CO2中,共价键的个数比为3:4 | |
| D. | 氧化剂与还原剂的物质的量之比为1:2时,NOx中氮元素的化合价为+4价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液呈橙色不分层 | B. | 溶液分两层,上层呈橙色 | ||
| C. | 溶液分两层,下层呈橙色 | D. | 溶液呈紫色不分层 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2H218O═4NaOH+18O2↑ | |
| B. | CH3COOH+CH3CH218OH→CH3COOCH2CH3+H218O | |
| C. | 5H218O2+2KMnO4+3H2SO4═518O2↑+K2SO4+2MnSO4+8H2O | |
| D. | K37ClO3+6HCl═K37Cl+3Cl2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
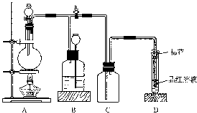 如图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置:
如图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com