
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如下图所示:
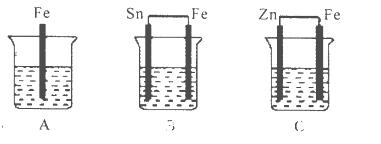
(1)A中反应的离子方程式是____________________________________
(2)B中Sn极的电极反应式为_________,Sn极附近溶液的酸性_________(填“增强”“减弱”或“不变”)。
(3) C中被腐蚀的金属是_________ ,比较A、B、C中铁被腐蚀的速率由快到慢的顺序是___________________________________
科目:高中化学 来源: 题型:
牙齿洁白,人人喜欢。将漂白剂沾在牙套上,牙齿咬住牙套可使牙齿变得洁白。下列物质溶于水后所得溶液可作为牙齿漂白剂的是 ( )。
A.Cl2 B.HNO3
C.Na2O2 D.H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列文字表述与反应方程式对应不正确的是( )
A. 氯气和水反应:Cl2 + H2O = 2H+ + Cl- + ClO-
B.用醋酸除去水垢:CaCO3 + 2CH3COOH = Ca2+ +2CH3COO-- + H2O + CO2↑
C.将丙烯通入溴水中:CH3—CH=CH2 + Br2→ CH3CHBrCH2Br
D.甲烷与氧气反应:CH4 + 2O2  CO2 + 2H2O
CO2 + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
卤族元素随着原子序数的增大,下列递变规律正确的是
A.原子半径逐渐增大 B.单质的氧化性逐渐增强
C.单质熔、沸点逐渐降低 D.气态氢化物稳定性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是—种性能优良的漂白剂,但遇酸性溶液发生分解:
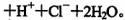 向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为硫酸,开始时反
向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为硫酸,开始时反
应缓慢,稍后—段时间产生气体速度较快,其原因可能是
A.逸出ClO2使生成物浓度降低 B.酸使亚氯酸的氧化性增强
C.溶液中的H+起催化作用 D.溶液中的Cl-起催化作用
查看答案和解析>>
科目:高中化学 来源: 题型:
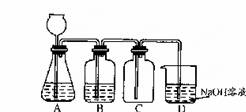
某小组利用MnO2和浓HCl以下图装置制备纯净C12。下列分析明显不正确的是( )
A、A中可用分液漏斗代替长颈漏斗
B.A处缺少加热装置
C.B中盛装NaOH溶液可以净化C12
D.D中的导管口连接倒置漏斗可防倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ、(7分)在一定条件下,将 2 molA 和 2 molB 混合于容积为 2L 的密闭容器中,发生如下反应:
3A ( g ) + B ( g )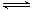 xC ( g ) + 2D ( g )。 2 min 末反应达到平衡状态时,生成 0.8molD ,同时测得 C 的浓度为 0.4 mol·L一1。请填写下列空白:
xC ( g ) + 2D ( g )。 2 min 末反应达到平衡状态时,生成 0.8molD ,同时测得 C 的浓度为 0.4 mol·L一1。请填写下列空白:
(1)x =_________;用 D 的浓度变化表示的化学反应速率为___________________
(2)A 的平衡浓度为_______________________ , B 的转化率为_____________。
(3)如果增大体系的压强,则平衡体系中 C 的体积分数将____________(填“增大”、“减小”或“不变”)。
Ⅱ、(12分)在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:CO2(g)+H2(g)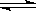 CO(g)+H2O(g)
CO(g)+H2O(g)
(1)该反应的化学平衡常数表达式K=________。
(2)已知在700 ℃时,该反应的平衡常数K1=0.6,则该温度下反应
CO(g)+H2O(g)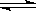 CO2(g)+H2(g)的平衡常数K2=________,
CO2(g)+H2(g)的平衡常数K2=________,
反应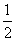 CO2(g)+
CO2(g)+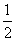 H2(g)
H2(g)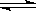
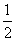 CO(g)+
CO(g)+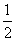 H2O(g)的平衡常数K3=________。
H2O(g)的平衡常数K3=________。
(3)已知在1 000 ℃时,该反应的平衡常数K4为1.0,则该反应为________反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是________。
A.容器中压强不变 B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2 D.混合气体的平均相对分子质量不变
(5)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v(正)________v(逆)(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种非 金属元素具有相同的电子层数,它们的气态氢化物的稳定性的强弱顺序为XH3<H2Y<HZ,则三种元素的非金属性和简单阴离子的还原性强弱顺序如何?
金属元素具有相同的电子层数,它们的气态氢化物的稳定性的强弱顺序为XH3<H2Y<HZ,则三种元素的非金属性和简单阴离子的还原性强弱顺序如何?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com