
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。
可选药品:稀硝酸、浓硝酸、浓硫酸、NaOH溶液、蒸馏水
查阅资料:
A.浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
B.氢氧化钠溶液不与NO反应,能与NO2反应2NO2 + 2NaOH = NaNO3 + NaNO2 +H2O
| 实验过程 | 实验现象 |
| I.检验装置的气密性 | |
| II.…… | |
| III.打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 | ①中产生大量的红棕色气体,红棕色气体在②中变为无色,气体通过③后依然为无色,通过④后变为红棕色 |
(1)Cu+4H++2NO3—== Cu2++2NO2↑+2H2O
(2)3NO2+ H2O == 2HNO3+ NO
(3)蒸馏水、稀硝酸、浓硝酸、氢氧化钠溶液
(4)打开弹簧夹,通一段时间N2,关闭弹簧夹 赶净装置中的空气(或氧气)
(5)③中液面上方为无色,④中液面上方变为红棕色
解析试题分析:(1)在①中Cu与浓硝酸发生反应:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O离子方程式是Cu+4H++2NO3—== Cu2++2NO2↑+2H2O.(2)②中发生反应的化学方程式是3NO2+ H2O == 2HNO3+ NO。(3)装置②~⑤中盛放的药品分别是②蒸馏水、③稀硝酸、④浓硝酸、⑤氢氧化钠溶液。(4)检验装置的气密性后进行的II的操作是打开弹簧夹,通一段时间N2,关闭弹簧夹,目的是赶净装置中的空气(或氧气)使整个系统处于惰性环境中,防止空气中的氧气把反应产生的NO氧化而影响实验结果的判断。(5)①中发生反应:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O,②中发生反应3NO2+ H2O == 2HNO3+ NO,③不反应,④中发生反应NO+2HNO3(浓)= 3NO2↑+H2O,⑤中发生反应2NO2 + 2NaOH = NaNO3 + NaNO2 +H2O.因此该同学得出结论所依据的实验现象是③中液面上方为无色,④中液面上方变为红棕色。
考点:考查浓、稀硝酸氧化性的相对强弱及离子方程式的书写、试剂使用的先后顺序等的知识。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:实验题
已知AgNO3晶体加热分解生成两种单质和红棕色气体。用下列某些装置粗略测定混入了其他不分解也不参与反应的杂质的硝酸银的纯度,并进行有关实验(装置中必要的铁架台、铁夹、酒精灯等已略去),填写下列空白。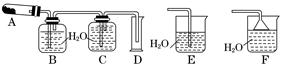
(1)写出AgNO3受热分解的化学方程式:_______________________________________________________________。
(2)测定AgNO3的纯度,可选用由A、B、C、D组成的装置,但其中不合理的是____________,该错误引起的后果是____________________________________________。
(3)B瓶中的空气对实验结果________(填“有”或“无”)影响,理由是____________________________________________________________________________。
(4)如果改进装置后,称取硝酸银试样4.00 g置于A中缓缓加热,待反应完全后,产生的气体通过B、C装置后,测得量筒中水的体积,并折算成标准状况下气体的体积为112 mL,则试样的纯度为________。
(5)如果加热Cu(NO3)2生成氧化铜,则加热分解所得气体应通入装置________(填“E”或“F”),其理由是__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
请分析回答某同学在探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铜反应的实验中发现的有关问题。
Ⅰ.探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质
(1)分别向盛有等量铜片的四支试管中加入等体积的浓硫酸、稀硫酸、浓硝酸、稀硝酸,实验结果记录如下表:
| | 酸 | 实验结果 |
| a | 浓硫酸 | 加热后发生反应,产生无色刺激性气体 |
| b | 稀硫酸 | 加热也不发生反应 |
| c | 浓硝酸 | 不加热即发生反应,产生红棕色气体 |
| d | 稀硝酸 | 微热发生反应,产生无色气体 |


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
工业上常用铁质容器盛装冷浓硫酸。某兴趣小组的同学发现:将一定量的生铁与浓硫酸加热时,观察到固体完全溶解,并产生大量气体。实验室现有下列试剂: 0.01 mol/L 酸性KMnO4溶液、0.10 mol/L KI溶液、新制氯水、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分。
【提出猜想】
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中肯定含有 气体。
【实验探究】
| | 实验操作 | 预期现象 | 结 论 |
| 验证猜想Ⅰ | 步骤①:取少量0.01 mol/L 酸性KMnO4溶液,滴入所得溶液中 | | |
| 步骤②: | | 含有Fe3+ | |
| 验证猜想Ⅱ | 将所得气体通入如下装置 | | 含有两种或以上气体 |


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。所用仪器如图: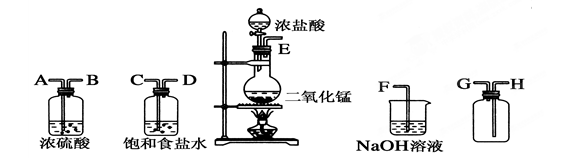
(1)连接上述仪器的正确顺序(填各接口处的字母):__接__;__接__;__接__;__接__。(2分)
(2)装置中,饱和食盐水的作用是______________;NaOH溶液的作用是____________。(4分)
(3)写出下列化学反应的方程式。
①气体发生装置中进行的反应:________________________________________。(2分)
②NaOH溶液中发生的反应:__________________________________________ 。(2分)
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某校化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数,并探究铁与浓硫酸的反应。
(1)m克铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是①常温下碳与浓硫酸不反应;② 。
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式 。
(3)B中的现象是: ;
C的作用是: 。
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。则铁碳合金中铁的质量分数为 (写含m、b的表达式)。
⑸反应一段时间后,用滴管吸取A中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
A:只含有Fe3+;B:只含有Fe2+;C: 。
验证C的实验方法是
。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某同学用下面的装置制备并收集纯净的氯化铁,硬质玻璃管E中装有细铁丝网。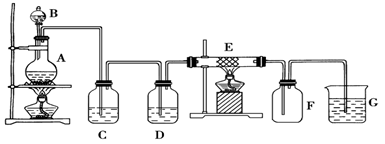
试回答:
(1)检验装置A的气密性的方法是
(2)装置A中反应的化学方程式为
(3)装置C的作用是: ________________,装置D中的试剂是:____ _______。
(4)可检验装置E中生成的物质中阳离子的方法及现象是 。
(5)若把氯气通入石蕊溶液中,观察的现象是: 。
(6)装置 G中发生反应的离子方程式为:________________ _ ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
Ⅰ、 (1)某化学兴趣小组欲从下列装置中选取必要的装置制取 (NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:a 
(2)将装置C中两种液体分离开的操作名称是__ _______。
装置D的作用是 。
Ⅱ、(4分)为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl)的工艺。某同学根据该原理设计的实验装置如图:
请回答下列问题:
(1) 装置A中发生反应生成碱式氯化镁的化学方程式为_________ ____
装置B中碱石灰的作用是_____ __
(2) 反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,二是_______________ ______
(3) 装置C的试管中反应的离子方程式为 ______________
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
已知Na2SO3固体与硫酸可发生反应:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,下图是实验室制取SO2并验证SO2的某些性质的装置图。试回答: [
[
(1)①中的实验现象为紫色石蕊试液_________________,此实验证明SO2是________气体。
(2)②中的品红溶液___________________,证明SO2有__________性。
(3)③中的实验现象是_________________,证明SO2有__________性。
(4)④中的实验现象是_________________,证明SO2有__________性。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com