
| A、25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| B、25℃时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
| C、25℃时,Mg(OH)2固体在20 mL 0.01 mol?L-1氨水中的Ksp比在20 mL 0.01 mol?L-1 NH4Cl溶液中的Ksp小 |
| D、25℃时,在MgF2的悬浊液加入NaOH溶液后,MgF2不可能转化成为Mg(OH)2 |


科目:高中化学 来源: 题型:
| A、铁强化酱油可通过膳食补充人体所需的铁元素 |
| B、变质的植物油有难闻的特殊气味,是由于植物油发生了水解反应 |
| C、一定浓度的双氧水可用于伤口的消毒 |
| D、蔬菜中含有维生素C,生吃新鲜蔬菜要比熟吃时维生素C的损失大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 通入O2 |
| 通入空气吹出Br2 |
| 用X吸收 |
| 通入Cl2 |
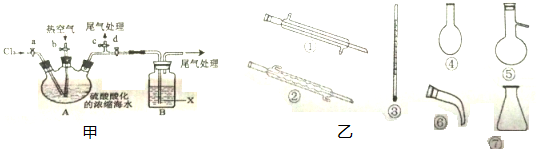
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、过滤操作时,玻璃棒与三层滤纸的一边接触 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、萃取操作时,一般选择有机萃取剂,且萃取剂必须与水不互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ |
| B、只有①②③ |
| C、只有①②③④ |
| D、只有①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
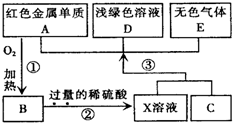 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
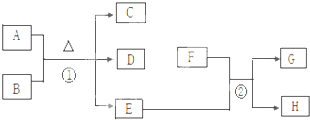 如图中A~H均为中学化学中常见的物质.已知A为紫红色金属,D能使品红溶液褪色,E为生活中常见的无色无味液体,F为黄绿色气体.请回答下列问题:
如图中A~H均为中学化学中常见的物质.已知A为紫红色金属,D能使品红溶液褪色,E为生活中常见的无色无味液体,F为黄绿色气体.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com