
【题目】(1)若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为___________.
(2)分子式为C9H20的某烃其一氯代物只有两种产物,写出符合要求的结构简式_______.
(3)分子式为C5H10的烯烃中不存在顺反异构的物质有________种.
(4)已知烯烃、炔烃在臭氧作用下发生以下反应:
CH3-CH=CH=CH=CH2![]() CH3CHO+OHC-CH2-CHO+HCHO
CH3CHO+OHC-CH2-CHO+HCHO
CH3-C![]() C-CH2-C
C-CH2-C![]() CH
CH![]() CH3COOH+HOOCCH2COOH+HCOOH
CH3COOH+HOOCCH2COOH+HCOOH
某烃化学式为C10H10,在臭氧作用下发生反应:
C10H10![]() CH3COOH+3HOOC-CHO+CH3CHO
CH3COOH+3HOOC-CHO+CH3CHO
①C10H10分子中含______个双键,______个三键。
②C10H10结构简式为____________.
【答案】CH3C![]() CCH3 (CH3)3CCH2C(CH3)3 4 2 2 CH3-C
CCH3 (CH3)3CCH2C(CH3)3 4 2 2 CH3-C![]() C-CH=CH-C
C-CH=CH-C![]() C-CH=CH-CH3
C-CH=CH-CH3
【解析】
考查有机物结构简式判断。同分异构体书写,(1)有机物中C2H2的空间构型为直线型,C4H6所有碳原子在一条直线上,该烃的结构简式为CH3C![]() CCH3 ;(2)C9H20为烷烃,一氯代物有2种,说明含有2种不同的氢原子,即结构简式为
CCH3 ;(2)C9H20为烷烃,一氯代物有2种,说明含有2种不同的氢原子,即结构简式为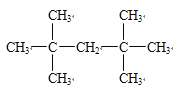 ;(3)C5H10的属于烯烃的同分异构体是CH2=CHCH2CH2CH3、CH3CH=CHCH2CH3、CH2=C(CH3)CH2CH3、(CH3)2C=CHCH2、(CH3)3CH=CH2,不存在顺反异构的是CH2=CHCH2CH2CH3、CH2=C(CH3)CH2CH3、(CH3)2C=CHCH2、(CH3)3CH=CH2,共有4种;(4)根据信息,碳碳叁键被氧化成羧基,碳碳双键被氧化成醛基,然后还原回去即可,结构简式为CH3-C
;(3)C5H10的属于烯烃的同分异构体是CH2=CHCH2CH2CH3、CH3CH=CHCH2CH3、CH2=C(CH3)CH2CH3、(CH3)2C=CHCH2、(CH3)3CH=CH2,不存在顺反异构的是CH2=CHCH2CH2CH3、CH2=C(CH3)CH2CH3、(CH3)2C=CHCH2、(CH3)3CH=CH2,共有4种;(4)根据信息,碳碳叁键被氧化成羧基,碳碳双键被氧化成醛基,然后还原回去即可,结构简式为CH3-C![]() C-CH=CH-C
C-CH=CH-C![]() C-CH=CH-CH3,①根据C10H10分子中有2个双键和2个三键;②根据上述分析,结构简式为CH3-C
C-CH=CH-CH3,①根据C10H10分子中有2个双键和2个三键;②根据上述分析,结构简式为CH3-C![]() C-CH=CH-C
C-CH=CH-C![]() C-CH=CH-CH3。
C-CH=CH-CH3。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】钛是一种重要的金属,以钛铁矿[主要成分为钛酸亚铁(FeTiO3),还含有少量Fe2O3]为原料制备钛的工艺流程如图所示。

(1)滤液1中钛元素以TiO2+形式存在,则“溶浸”过程发生的主要反应的化学方程式为________。
(2)物质A为________(填化学式),“一系列操作”为________。
(3)“水解”步骤中生成TiO2·xH2O,为提高TiO2·xH2O的产率,可采取的措施有________、________。(写出两条)。
(4)“电解”是以石墨为阳极,TiO2为阴极,熔融CaO为电解质。阴极的电极反应式为________;若制得金属Ti 9.60g,阳极产生气体________mL(标准状况下)。
(5)将少量FeSO4·7H2O溶于水,加入一定量的NaHCO3溶液,可制得FeCO3,写出反应的离子方程式________;若反应后的溶液中c(Fe2+)=2×10-6mol·L-1,则溶液中c(CO32-)=________mol·L-1。(已知:常温下FeCO3饱和溶液浓度为4.5×10-6mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda﹣style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
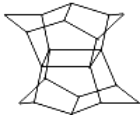
A. 分子式为C20H20
B. 一氯代物的同分异构体只有两种
C. 分子中含有二个亚甲基(﹣CH2﹣)
D. 分子中含有4个五元碳环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四种元素:Fe、O、S、H,由这四种元素中的一种或几种组成许多物质。回答下列问题:
(1)写出这些物质中符合下列要求的化学式(只写一种):
酸性氧化物_______,无氧酸_______,正盐_______。
(2)写出这些物质中符合下列要求的反应的化学方程式:
金属单质与非金属单质_______。
碱性氧化物和含氧酸_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是________,证明Fe3+存在的现象是________。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式:________。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式。
①________,④________。
(4)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为________。
①加入足量氯水②加入足量KMnO4溶液③加入少量KSCN溶液
A.①③ B.③② C.③① D.①②③
(5)写出向②⑤的混合液中通入⑥的离子方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.硫是一种不溶于水的淡黄色固体
B.硫与非金属反应时一定作还原剂
C.硫与铁反应时生成硫化铁
D.硫在自然界中仅以化合态存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是力学、化学综合性能良好的合金,广泛应用于制造高级弹性元件。以下是从某废旧铍铜元件(含BeO、CuS、少量FeS和SiO2)中回收铍和铜两种金属的流程。

已知:Ⅰ.铍、铝元素处于周期表中的对角线位置,化学性质相似
Ⅱ.常温下:Ksp[Cu(OH)2]、=2.2×10-20、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Mn(OH)2]=2.l×10-13
(1)写出铍铜元件中SiO2与NaOH溶液反应的离子方程式______________________。
(2)滤渣B的主要成分为___________________(填化学式)。写出反应Ⅰ中含铍化合物与过量盐酸反应的化学方程式___________________________________________。
(3)①溶液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,选择合理步骤并排序________。
a.加入过量的NaOH b.过滤 c.加入适量的HCl
d.加入过量的氨水 e.通入过量的CO2 f.洗涤
②从BeCl2溶液中得到BeCl2固体的操作是___________________________________。
(4)MnO2能将金属硫化物中的硫元素氧化为单质硫,写出反应Ⅱ中CuS发生反应的离子方程式________________________________。
(5)溶液D中含c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入稀氨水调节pH可依次分离,首先沉淀的是___________(填离子符号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com