
| A. | 氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)] | |
| B. | Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2 c(H2CO3) | |
| C. | 等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) | |
| D. | 室温下,向0.01 mol•L-1 NH4HSO4溶液中滴加NaOH溶液至中性:c(NH4+)>c(Na+)>c(SO42-)>c(OH-)=c(H+) |
分析 A.通入Cl2的物质的量=2[n(ClO-)+n(Cl-)+n(HClO)]+n(Cl2);
B.根据碳酸钠溶液中的质子守恒判断;
C.根据次氯酸钠、碳酸氢钠溶液中的物料守恒判断;
D.溶液呈中性时,溶液中存在铵根离子和一水合氨,则c(Na+)>c(SO42-)>c(NH4+)、c(OH-)=c(H+).
解答 解:A.氯气溶于水后,部分氯气与水反应生成氯化氢和次氯酸,氯化氢完全电离,次氯酸部分电离,则通入Cl2的物质的量=2[n(ClO-)+n(Cl-)+n(HClO)]+n(Cl2),而不是c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)],故A错误;
B.Na2CO3溶液中存在质子守恒:c(OH-)=c(H+)+c(HCO3-)+2 c(H2CO3),整理可得:c(OH-)-c(H+)=c(HCO3-)+2 c(H2CO3),故B正确;
C.等浓度的NaClO、NaHCO3混合溶液中,根据物料守恒可得:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-),故C错误;
D.向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,溶质为等物质的量的(NH4)2SO 4和Na2SO 4,溶液呈酸性,再滴加少许NaOH呈中性,溶液中正确的离子浓度大小为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),故D错误;
故选B.
点评 本题考查了离子浓度大小比较,题目难度中等,注意掌握物料守恒、电荷守恒及盐的水解原理的含义及应用方法,A为易错点,试题培养了学生的分析能力及灵活应用能力.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:实验题
 请根据化学反应Fe+CuCl2=FeCl2+Cu设计一个原电池.限选材料CuCl2(aq),FeCl2 (aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线.
请根据化学反应Fe+CuCl2=FeCl2+Cu设计一个原电池.限选材料CuCl2(aq),FeCl2 (aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | |||
| T | Q | W | |
| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | T的氧化物属于两性氧化物 | |
| D. | W的氧化物对应的水化物一定是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A和B的总能量一定高于C和D的总能量 | |
| B. | A的能量一定低于C的,B的能量一定低于D的 | |
| C. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| D. | 破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
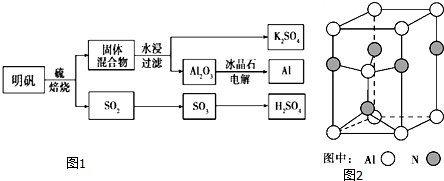
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 6种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH $→_{170℃}^{浓H_{2}SO_{4}}$ C2H4↑+H2O | |
| B. | 2CH3CHO+O2 $\stackrel{催化剂}{→}$2CH3COOH | |
| C. | CH3-CH=CH2+Br2→CH3-CHBr-CH2Br | |
| D. |  +Br2 $\stackrel{Fe}{→}$ +Br2 $\stackrel{Fe}{→}$ 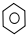 -Br+HBr -Br+HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液化石油气、汽油、柴油和润滑油的主要成分都是碳氢化合物 | |
| B. | 乙烯、氯乙烯和聚氯乙烯都能因发生加成反应而使溴水褪色 | |
| C. | 用溴水既可以鉴别甲烷和乙烯.也可以除去甲烷中的乙烯 | |
| D. | 可以通过灼烧时的特殊气味来鉴别蛋自质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com