
分类是化学学习与研究的常用方法,下列分类正确的是( )
A.C l2O7、P2O5、SO3、CO2均属于酸性氧化物
l2O7、P2O5、SO3、CO2均属于酸性氧化物
B.Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质
科目:高中化学 来源:2017届内蒙古高三上月考二化学试卷(解析版) 题型:选择题
下列关于氧化还原反应说法正确的是
A.肯定一种元素被氧化,另一种元素被还原
B.某元素从化合态变成游离态,该元素一定被还原
C.在反应中不一定所有元素的化合价都发生变化
D.在氧化还原反应中非金属单质一定是氧化剂
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、AlO2-、CO32-、SiO32-、Cl-中的几种,现进行如下实验:
①取少量溶液加氢氧化钠溶液过程中无沉淀生成
②另取少量原溶液,逐滴加入5 mL0.2 mol·L-1盐酸,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生 气体,最后沉淀逐渐减少至消失。
气体,最后沉淀逐渐减少至消失。
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.43 g。
下列说法中正确的是:( )
A.该溶液中一定不含 Ba2+ 、Mg2+、A13+、SiO32-、Cl-
Ba2+ 、Mg2+、A13+、SiO32-、Cl-
B.该溶液中一定含有K+、AlO2-、CO32-、Cl-
C.该溶液是否有K+ 需做焰色反应(透过蓝色钴玻璃片)
D.可能含有Cl-
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
设NA为阿伏加罗常数的值,下列说法正确的是( )
A.1molMg在空气中完全燃烧生成MgO和Mg 3N2,转移的电子数为NA
3N2,转移的电子数为NA
B.14g分子式为CnH2n的链烃中含有的C—H键的数目为2NA
C.室温时,1.0LpH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA
D.Fe与水蒸汽反应生成22.4L氢气,转移电 子数为2NA
子数为2NA
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟二化学试卷(解析版) 题型:选择题
常温下,将一定量的氯气通入100mL 4mol/L的氢氧化钠溶液中,发生反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O.充分反应后,下列说法正确的是(NA为阿伏加德罗常数)( )
A.当通入的Cl2为2.24 L时,反应中电子转移数目为0.1 NA
B.当溶液中Na+为0.4 NA时,溶液中的Cl﹣为0.2 NA
C.当电子转移数目为0.2 NA时,溶液质量增加7.1 g
D.当溶液质量增加7.1 g时,溶液中ClO﹣约为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
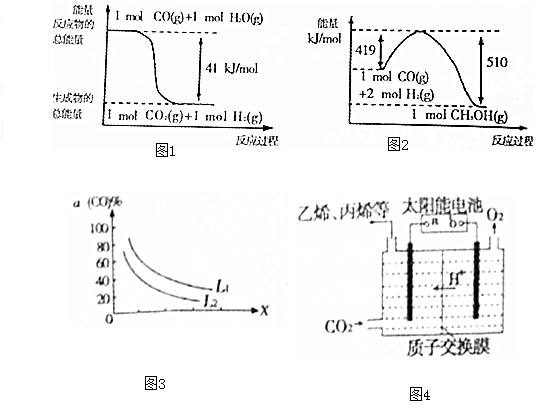
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol•L-1) | 0.46 | 1.0 | 1.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
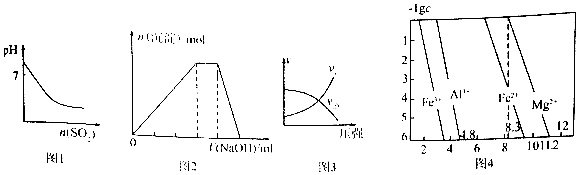
| A. | 图1表示常温下,将SO2气体通入溴水中,所得溶液pH的变化 | |
| B. | 图2表示向NH4A1(SO4)2溶液中逐滴滴入NaOH溶液,沉淀总物质的量(n)随NaOH溶液体积(V)的变化 | |
| C. | 图3表示T°C时,对于可逆反应:A(g)+B(g)?2C(g)+D(g)△H>0,正、逆反应速率与压强的关系 | |
| D. | 图4表示常温下,几种难溶氢氧化物的饱和溶液中金属离子浓度的负对数与溶液PH的关系,则在pH=7的溶液中,Fe3+、A13+、Fe2+能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com