
ЎѕМвДїЎїКµСйКТїЙУГ№ММе¶юСх»ЇГМУлЕЁСОЛбФЪјУИИМхјюПВЦЖИЎВИЖшЈ¬»ЇС§·ЅіМКЅОЄMnO2+4HCl(ЕЁ)![]() MnCl2+Cl2Ўь+2H2OЈ¬ТСЦЄЕЁСОЛбТЧ»У·ўЎЈДіС§ЙъЙијЖИзПВНјЛщКѕµДКµСйЧ°ЦГЈ¬АыУГВИЖшУлі±КЄµДКмКЇ»Т·ґУ¦ЦЖИЎЙЩБїЖЇ°Ч·Ы(ХвКЗТ»ёц·ЕИИ·ґУ¦)ЎЈ»ШґрПВБРОКМвЈє
MnCl2+Cl2Ўь+2H2OЈ¬ТСЦЄЕЁСОЛбТЧ»У·ўЎЈДіС§ЙъЙијЖИзПВНјЛщКѕµДКµСйЧ°ЦГЈ¬АыУГВИЖшУлі±КЄµДКмКЇ»Т·ґУ¦ЦЖИЎЙЩБїЖЇ°Ч·Ы(ХвКЗТ»ёц·ЕИИ·ґУ¦)ЎЈ»ШґрПВБРОКМвЈє
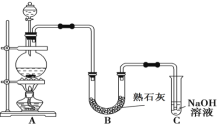
(1)AЧ°ЦГОЄКµСйКТЦЖИЎВИЖшµДЧ°ЦГЈ¬AЧ°ЦГЦР·ґУ¦µДАлЧУ·ЅіМКЅОЄ__________________ЎЈ
(2)ЖЇ°Ч·ЫЅ«ФЪUРО№ЬЦРІъЙъЈ¬Жд»ЇС§·ЅіМКЅКЗ___________________________________ЎЈ
(3)CЧ°ЦГµДЧчУГКЗ____________________ЎЈ
(4)ґЛКµСйЛщµГЖЇ°Ч·ЫµДУРР§іЙ·ЦЖ«µНЈ¬ёГС§Йъѕ·ЦОцІўІйФДЧКБП·ўПЦЈ¬ЦчТЄФТтКЗФЪUРО№ЬЦР»№ґжФЪБЅёцё±·ґУ¦ЎЈ
ўЩОВ¶ИЅПёЯК±ВИЖшУлКмКЇ»Т·ґУ¦ЙъіЙCa(ClO3)2Ј¬ОЄ±ЬГвґЛё±·ґУ¦µД·ўЙъЈ¬їЙІЙИЎµДґлК©КЗ____________________ЎЈ
ўЪКФЕР¶ПБнТ»ёцё±·ґУ¦_____________________________________(УГ»ЇС§·ЅіМКЅ±нКѕ)ЎЈ
Ўѕґр°ёЎїMnO2+4H+ + 2Cl- ![]() Mn2+ +Cl2Ўь+2H2O 2Cl2 + 2Ca(OH)2 == Ca(ClO)2 + CaCl2 + 2H2O ОьКХ¶аУаВИЖшЈ¬·АЦ№ОЫИѕїХЖш Ѕ«BЧ°ЦГ·ЕИлАдЛ®ЦР 2HCl+Ca(OH)2 == CaCl2 + 2H2O
Mn2+ +Cl2Ўь+2H2O 2Cl2 + 2Ca(OH)2 == Ca(ClO)2 + CaCl2 + 2H2O ОьКХ¶аУаВИЖшЈ¬·АЦ№ОЫИѕїХЖш Ѕ«BЧ°ЦГ·ЕИлАдЛ®ЦР 2HCl+Ca(OH)2 == CaCl2 + 2H2O
ЎѕЅвОцЎї
ЈЁ1Ј©КµСйКТїЙУГ№ММе¶юСх»ЇГМУлЕЁСОЛбФЪјУИИМхјюПВЦЖИЎВИЖшЈ¬»ЇС§·ЅіМКЅОЄMnO2+4HCl(ЕЁ)![]() MnCl2+Cl2Ўь+2H2OЈ¬ѕЭґЛРґіцАлЧУ·ЅіМКЅЈ»
MnCl2+Cl2Ўь+2H2OЈ¬ѕЭґЛРґіцАлЧУ·ЅіМКЅЈ»
ЈЁ2Ј©ВИЖшУлКмКЇ»Т·ґУ¦ЙъіЙґОВИЛбёЖЎўВИ»ЇёЖєНЛ®Ј¬ѕЭґЛРґіц»ЇС§·ЅіМКЅЈ»
ЈЁ3Ј©CЧ°ЦГЦРКў·ЕЗвСх»ЇДЖИЬТєЈ¬їЙТФОьКХ¶аУаµДВИЖшЈ¬·АЦ№ОЫИѕїХЖшЈ»
ЈЁ4Ј©ўЩОВ¶ИЅПёЯК±ВИЖшУлКмКЇ»Т·ґУ¦ЙъіЙCa(ClO3)2Ј¬ОЄ±ЬГвґЛё±·ґУ¦µД·ўЙъЈ¬У¦ёГЅµµНОВ¶ИЈ¬їЙЅ«BЧ°ЦГ·ЕИлАдЛ®ЦРЈ»
ўЪСОЛбТЧ»У·ўЈ¬јУИИ№эіМЦРЙъіЙµДВИЖшЦРє¬УРВИ»ЇЗвЈ¬ВИ»ЇЗвДЬУлЗвСх»ЇёЖ·ґУ¦ЎЈ
ЈЁ1Ј©КµСйКТїЙУГ№ММе¶юСх»ЇГМУлЕЁСОЛбФЪјУИИМхјюПВЦЖИЎВИЖшЈ¬»ЇС§·ЅіМКЅОЄMnO2+4HCl(ЕЁ)![]() MnCl2+Cl2Ўь+2H2OЈ¬АлЧУ·ЅіМКЅОЄMnO2+4H+ + 2Cl-
MnCl2+Cl2Ўь+2H2OЈ¬АлЧУ·ЅіМКЅОЄMnO2+4H+ + 2Cl-![]() Mn2+ +Cl2Ўь+2H2OЈ»
Mn2+ +Cl2Ўь+2H2OЈ»
№Кґр°ёОЄЈєMnO2+4H+ + 2Cl-![]() Mn2+ +Cl2Ўь+2H2OЈ»
Mn2+ +Cl2Ўь+2H2OЈ»
ЈЁ2Ј©ВИЖшУлКмКЇ»Т·ґУ¦ЙъіЙґОВИЛбёЖЎўВИ»ЇёЖєНЛ®Ј¬Жд»ЇС§·ЅіМКЅКЗ2Cl2 + 2Ca(OH)2 == Ca(ClO)2 + CaCl2 + 2H2OЈ»
№Кґр°ёОЄЈє2Cl2 + 2Ca(OH)2 == Ca(ClO)2 + CaCl2 + 2H2OЈ»
ЈЁ3Ј©CЧ°ЦГЦРКў·ЕЗвСх»ЇДЖИЬТєЈ¬їЙТФОьКХ¶аУаµДВИЖшЈ¬·АЦ№ОЫИѕїХЖшЈ¬ФтCЧ°ЦГµДЧчУГКЗОьКХВИЖшЈ¬·АЦ№ОЫИѕґуЖшЈ»
№Кґр°ёОЄЈєОьКХ¶аУаВИЖшЈ¬·АЦ№ОЫИѕїХЖшЈ»
(4)ўЩОВ¶ИЅПёЯК±ВИЖшУлКмКЇ»Т·ґУ¦ЙъіЙCa(ClO3)2Ј¬ОЄ±ЬГвґЛё±·ґУ¦µД·ўЙъЈ¬У¦ёГЅµµНОВ¶ИЈ¬їЙІЙИЎµДґлК©КЗЅ«BЧ°ЦГ·ЕИлАдЛ®ЦРЈ¬·АЦ№ОВ¶И№эёЯЙъіЙCa(ClO3)2Ј»
№Кґр°ёОЄЈєЅ«BЧ°ЦГ·ЕИлАдЛ®ЦРЈ»
ўЪСОЛбТЧ»У·ўЈ¬јУИИ№эіМЦРЙъіЙµДВИЖшЦРє¬УРВИ»ЇЗвЈ¬ВИ»ЇЗвДЬУлЗвСх»ЇёЖ·ґУ¦Ј¬ЛщТФБнТ»ёцё±·ґУ¦µД»ЇС§·ЅіМКЅКЗ2HCl+Ca(OH)2 == CaCl2 + 2H2OЈ»
№Кґр°ёОЄЈє2HCl+Ca(OH)2 == CaCl2 + 2H2OЎЈ


 Т»ЕµКйТµКојЩЧчТµїмАЦјЩЖЪФЖДПГАКхіц°жЙзПµБРґр°ё
Т»ЕµКйТµКојЩЧчТµїмАЦјЩЖЪФЖДПГАКхіц°жЙзПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїТФCO2єНNa2O2ОЄФБПЈ¬ЦЖИЎґїѕ»ёЙФпµДO2Ј¬КµСйЧ°ЦГИзПВЈє

ПВБРЛµ·ЁІ»ХэИ·µДКЗ
A. Ч°ЦГўЪЦРКФјБїЙТФКЗNaOHИЬТє
B. Ч°ЦГўЫµДЧчУГКЗёЙФпO2
C. КХјЇСхЖшУ¦СЎФсЧ°ЦГa
D. Ч°ЦГўЪЎўўЫЦ®јдУ¦ФцјУКўіОЗеКЇ»ТЛ®µДПґЖшЖї
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїОшКЗ¶ЇОпєНИЛМеЛщ±ШРиµДОўБїФЄЛШЦ®Т»Ј¬ТІКЗТ»ЦЦЦШТЄµД№¤ТµФБПЎЈОшФЪЧФИ»ЅзЦРПЎЙЩ¶ш·ЦЙўЈ¬іЈґУѕ«Б¶НµДСфј«ДаЦРМбИЎОшЎЈ
ЈЁ1Ј©ґЦНѕ«Б¶К±Ј¬НЁіЈУГѕ«НЧч____ј«ЈЁМоЎ°ТхЎ±»тЎ°СфЎ±Ј©ЎЈ
ЈЁ2Ј©ОшФЪФЄЛШЦЬЖЪ±нЦРµДО»ЦГИзНјЛщКѕЈє

SeФЧУЅб№№КѕТвНјїЙ±нКѕОЄ________ЎЈ
ўЪґУФЧУЅб№№ЅЗ¶ИЅвКНБтУлОшФЄЛШРФЦКПаЛЖУлІ»Н¬µДФТтЈєН¬Т»ЦчЧе________ЎЈ
ЈЁ3Ј©Сфј«ДаЦРµДОшЦчТЄТФSeєНCuSeµДРОКЅґжФЪЈ¬№¤ТµЙПіЈУГБтЛб»Ї±єЙХ·ЁМбИЎОшЈ¬ЦчТЄІЅЦиИзПВЈє
iЈ®Ѕ«є¬ОшСфј«ДаУлЕЁБтЛб»мєП±єЙХЈ¬ІъЙъSO2ЎўSeO2µД»мєПЖшМе
iiЈ®УГЛ®ОьКХiЦР»мєПЖшМеЈ¬їЙµГSe№ММе
ўЩ ЗлРґіцCuSeУлЕЁH2SO4·ґУ¦µД»ЇС§·ЅіМКЅ________ЎЈ
ўЪ ±єЙХ№эіМІъЙъµДСМЖшЦРє¬УРЙЩБїSeO2Ј¬їЙУГNaOHИЬТєОьКХЈ¬¶юХЯ·ґУ¦ЙъіЙТ»ЦЦСОЈ¬ёГСОµД»ЇС§КЅОЄ_______ЎЈ
ўЫ РґіцІЅЦиўўЦРµД»ЇС§·ЅіМКЅ_______ЎЈ
ЈЁ4Ј©ПВБРЛµ·ЁєПАнµДКЗ________ЎЈ
a. SeO2јИУРСх»ЇРФУЦУР»№ФРФЈ¬Жд»№ФРФ±ИSO2Зї
b. ЕЁОшЛбїЙДЬѕЯУРЗїСх»ЇРФЎўНСЛ®РФ
c. ИИОИ¶ЁРФЈєH2Se < HCl < H2S
d. ЛбРФЈєH2SeO4 < HBrO4 < HClO4
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЅ«µИОпЦКµДБїµДXЎўYЖшМеідИлТ»ёцГЬ±ХИЭЖчЦРЈ¬ФЪТ»¶ЁМхјюПВ·ўЙъИзПВ·ґУ¦ІўґпµЅЖЅєвЈєX(g)Ј«Y(g) ![]() 2Z(g)ЎЎ¦¤H<0ЎЈµ±ёД±дДіёцМхјюІўґпµЅРВЖЅєвєуЈ¬ПВБРРрКцХэИ·µДКЗ(ЎЎЎЎ)
2Z(g)ЎЎ¦¤H<0ЎЈµ±ёД±дДіёцМхјюІўґпµЅРВЖЅєвєуЈ¬ПВБРРрКцХэИ·µДКЗ(ЎЎЎЎ)
A. ЙэёЯОВ¶ИЈ¬XµДМе»э·ЦКэјхРЎ
B. ФцґуС№Зї(ЛхРЎИЭЖчМе»э)Ј¬ZµДЕЁ¶ИІ»±д
C. ±ЈіЦИЭЖчМе»эІ»±дЈ¬ідИлТ»¶ЁБїµД¶иРФЖшМеЈ¬YµДЕЁ¶ИІ»±д
D. ±ЈіЦИЭЖчМе»эІ»±дЈ¬ідИлТ»¶ЁБїµДZЈ¬XµДМе»э·ЦКэФцґу
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїXЎўYЎўZИэЦЦЖшМе¶јДЬ¶ФґуЖшФміЙОЫИѕЈ¬ФЪ№¤ТµЙП¶јїЙТФУГјоТєОьКХЎЈТСЦЄXКЗ»ЇКЇИјБПИјЙХІъОпЦ®Т»Ј¬КЗРОіЙЛбУкµДЦчТЄОпЦКЈ»YКЗТ»ЦЦµҐЦКЈ¬ЛьµДЛ®ИЬТєѕЯУРЖЇ°ЧЧчУГЈ»ZКЗПхЛṤҵєНЖыіµОІЖшЦРµДУРє¦ОпЦКЦ®Т»Ј¬ДЬУлЛ®·ґУ¦ЎЈЗлРґіцПВБРОпЦК·ґУ¦µД»ЇС§·ЅіМКЅЎЈ
(1)XФЪТ»¶ЁМхјюПВУлСхЖш·ґУ¦____________________________________Ј»
(2)YУлЗвСх»ЇДЖИЬТєµД·ґУ¦______________________________________Ј»
(3)ZУлЛ®µД·ґУ¦________________________________________________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЅЎїµИЛМеДЪє¬МъФЄЛШґуФј 2~3gЈ¬ИЛМеДЪМъФЄЛШТФСЗМъАлЧУєНИэјЫМъАлЧУµДРОКЅґжФЪЈ¬Fe2+ТЧ±»ОьКХЈ¬ЛщТФёшЖ¶СЄХЯІ№ідМъФЄЛШК±Ј¬У¦І№ідє¬ Fe2+µДСЗМъСОЎЈЎ°ЛЩБ¦·ЖЎ±ЈЁЦчТЄіЙ·ЦЈєзъзкЛбСЗМъЈ¬іК°µ»ЖЙ«Ј©КЗКРіЎЙПТ»ЦЦіЈјыµДІ№МъТ©ОпЎЈёГТ©Ж·І»ИЬУЪЛ®µ«ДЬИЬУЪИЛМеЦРµДОёЛбЎЈДіН¬С§ОЄБЛјмІвЎ°ЛЩБ¦·ЖЎ±Т©Ж¬ЦРFe2+µДґжФЪЈ¬ЙијЖІўЅшРРБЛИзПВКµСйЈє

(1) КФјБ1µДГыіЖКЗ__________Ј»КФјБ2µД»ЇС§КЅОЄ______________ЎЈ
(2) јУИлРВЦЖВИЛ®Ј¬ИЬТєЦР·ўЙъ·ґУ¦µДАлЧУ·ЅіМКЅКЗ_____________________________ЎЈ
(3) јУИлКФјБ2 К±ИЬТєОЄµємЙ«ЛµГч Ў°ЛЩБ¦·ЖЎ±ЦРµД Fe2+ТСІї·ЦСх»ЇЈ¬Т»°гФЪ·юУГЎ°ЛЩБ¦·ЖЎ±К±Ј¬Н¬К±·юУГО¬ЙъЛШCЈ¬ЛµГчО¬ЙъЛШCѕЯУР___________РФЎЈ
(4) І»ЅцИЬТєЦРFe2+ТЧ±»Сх»ЇіЙFe3+Ј¬ИЬТєЦР°ЧЙ«іБµнFe(OH)2ёьТЧ±»O2Сх»ЇЈ¬ЗлРґіц·ґУ¦µД»ЇС§·ЅіМКЅ________________________Ј¬ПЦПуОЄ__________________________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїє¬µЄ»ЇєПОпУлЙъІъЎўЙъ»оЎўЙъГьєН»·ѕіПўПўПа№ШЎЈ
(1)NOјУЛЩіфСхІг±»ЖЖ»µЈ¬Жд·ґУ¦№эіМИзНјЛщКѕЎЈ
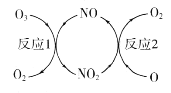
ўЩNOµДЧчУГКЗ________________________ЎЈ
ўЪТСЦЄЈєO3(g)+O(g) ЈЅ2O2(g) ЎчH=-143kJЎ¤mol-1
·ґУ¦lЈєO3(g)+NO(g) ЈЅNO2(g)+O2(g)ЎчH1=-200.2kJЎ¤mol-1
Фт·ґУ¦2µДИИ»ЇС§·ЅіМКЅОЄ____________________________ЎЈ
(2)јЎємµ°°Ч(Mb)КЗјЎИвДЪґўґжСхµДµ°°ЧЦКЈ¬№№іЙјЎємµ°°ЧµДёК°±Лб(H2NCH2COOH)КЗТ»ЦЦБЅРФОпЦКЈ¬ФЪИЬТєЦРТФИэЦЦАлЧУРОКЅґжФЪЈ¬ЖдЧЄ»Ї№ШПµИзПВ ИэЦЦАлЧУµДОпЦКµДБї·ЦКэ(¦Д)Ул[
ИэЦЦАлЧУµДОпЦКµДБї·ЦКэ(¦Д)Ул[![]() ]µД№ШПµИзНјЛщКѕЎЈ
]µД№ШПµИзНјЛщКѕЎЈ

ўЩИЬТєіКЦРРФК±Ј¬ИэЦЦАлЧУЕЁ¶ИУЙґуµЅРЎµДЛіРтОЄ______________________ЎЈ
ўЪПтAG=12µДИЬТєЦРјУИл№эБїNaOHИЬТєК±Ј¬ЦчТЄ·ґУ¦µДАлЧУ·ЅіМКЅОЄ______________ЎЈ
(3)јЎємµ°°Ч(Mb)їЙУлO2ЅбєПЙъіЙMbO2Јє![]() ЎЈ37ЎжК±ІвµГјЎємµ°°ЧµДЅбєП¶И(¦Б)Улp(O2)µД№ШПµИзПВ±нЎЈ
ЎЈ37ЎжК±ІвµГјЎємµ°°ЧµДЅбєП¶И(¦Б)Улp(O2)µД№ШПµИзПВ±нЎЈ
[ЅбєП¶И(¦Б)ЦёТСУлO2ЅбєПµДјЎємµ°°ЧХјЧЬјЎємµ°°ЧµДОпЦКµДБї·ЦКэ]
p(O2)ЈЇkPa | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
¦Б(MbO2)% | 50.0 | 66.7 | 80.0 | 85.7 | 88.9 | 90.9 | 92.3 |
ўЩјЖЛг37ЎжК±Ј¬ЙПКц·ґУ¦µДЖЅєвіЈКэK=__________kPa-1(ЖшМеєНИЬТєЦРµДИЬЦК·Ц±рУГ·ЦС№єНОпЦКµДБїЕЁ¶И±нКѕ)ЎЈ
ўЪ37ЎжК±Ј¬ИфїХЖшЦРСхЖш·ЦС№ОЄ21.0 kPaЈ¬ФтИЛХэіЈєфОьК±¦БµДЧоґуЦµОЄ________ЈҐ(±ЈБф1О»РЎКэ)ЎЈ
ўЫОВ¶ИІ»±дК±Ј¬УОїНФЪЙЅ¶ҐК±МеДЪMbO2µДЕЁ¶И±ИФЪЙЅПВ________(МоЎ°ёЯЎ±»тЎ°µНЎ±)ЎЈ
ўЬСРѕї·ўПЦЈ¬vХэ=kХэЎ¤c(Mb)Ў¤p(O
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї№¤ТµЦЖЗвЖшµДТ»ёцЦШТЄ·ґУ¦КЗЈєCO(g) +H2O(g)== CO2(g)+H2(g)ЎЈ
ТСЦЄФЪ25ЎжК±Јє
ўЩC(s)+![]() O2(g)
O2(g)![]() CO(g) ¦¤H1ЈЅ111kJЎ¤mol 1
CO(g) ¦¤H1ЈЅ111kJЎ¤mol 1
ўЪH2(g)+![]() O2(g)== H2O(g) ¦¤H2ЈЅ242kJЎ¤mol 1
O2(g)== H2O(g) ¦¤H2ЈЅ242kJЎ¤mol 1
ўЫC(s)+O2(g) == CO2(g) ¦¤H3ЈЅ394kJЎ¤mol 1
ПВБРЛµ·ЁІ»ХэИ·µДКЗ
A. 25ЎжК±Ј¬CO(g)+H2O(g)==CO2(g)+H2(g) ¦¤HЈЅ41kJЎ¤mol1
B. ФцґуС№ЗїЈ¬·ґУ¦ўЩµДЖЅєвПтДж·ґУ¦·ЅПтТЖ¶ЇЈ¬ЖЅєвіЈКэKјхРЎ
C. ·ґУ¦ўЩґпµЅЖЅєвК±Ј¬ГїЙъіЙ1molCOµДН¬К±ЙъіЙ0.5molO2
D. ·ґУ¦ўЪ¶ПїЄ2molH2єН1molO2ЦРµД»ЇС§јьЛщОьКХµДДЬБї±ИРОіЙ4molO-HјьЛщ·ЕіцµДДЬБїЙЩ484kJ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїКµСйКТПт 0.783g MnO2 ЦРјУИл 20mL36.5%ЈЁ¦С=1.18g/cm3 Ј©ЕЁСОЛбєуЈ¬№ІИИЦЖИЎ Cl2Ј®·ґУ¦·ЅіМКЅОЄЈєMnO2+4HClMnCl2+Cl2+2H2OЈ¬Иф·ґУ¦єуИЬТєМе»эИФОЄ 20mLЈ¬ФтПВБРЛµ·ЁХэИ·µДКЗЈЁЎЎЎЎЈ©
A.·ґУ¦ПыєД HCl ОпЦКµДБїОЄ 0.236mol
B.·ґУ¦ЙъіЙ Cl2 ЖшМеµДМе»эОЄ 201.6mL
C.ИфИЎ 2mL ·ґУ¦єуµДИЬТєЈ¬јУИлЧгБї AgNO3Ј¬їЙІъЙъіБµн 2.87g
D.ИфИЎ 2mL ·ґУ¦єуµДИЬТєЈ¬јУИл 2.0mol/L µД NaOHЈ¬µ±іБµнґпµЅЧоґуЦµК±Ј¬ПыєД NaOH ИЬТєµДМе»эОЄ10.9mL
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com