
【题目】某研究性学习小组的同学想通过下图实验装置探究SO2与Na2O2反应的产物。(夹持装置已略去,装置的气密性良好)
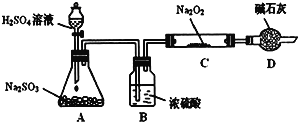
Ⅰ.实验中装置B可吸收水分,干燥SO2气体,其目的是:_________________________。装置D除了吸收过量的SO2,避免污染空气外,还起到的作用是:_________________。
Ⅱ.对C中固体产物提出如下假设:(假设Na2O2已全部反应)
假设1:__________。 假设2:只有Na2SO4; 假设3:既有Na2SO3又有Na2SO4。
(1)甲同学认为SO2与Na2O2的反应不同于CO2,应为假设2成立,请据此写出C中所发生反应的化学方程式:_____________________。
(2)若假设2成立,为确定C中固体产物的成分,甲同学设计如下实验:
![]()
得出结论:C中固体产物只有Na2SO4。该方案是否合理?答:__________。(填“是”或“否”)理由是______________________________。
(3)乙同学为证明假设3成立,设计如下实验。
实验步骤和结论为:
①取少量C中固体产物于试管中,加入适量的蒸馏水溶解;
②滴加过量的1molL-1BaCl2溶液,若产生白色沉淀,则证明C中固体产物中有_________;
③滴加适量的1molL-1稀盐酸,若白色沉淀部分溶解,并产生刺激性气味气体,则证明C中固体产物中有___________________。
【答案】 防止水蒸气与Na2O2反应 防止空气中的水和CO2进入玻璃管C 只有Na2SO3 SO2+Na2O2=Na2SO4。 否 NO3-在酸性条件下可将BaSO3氧化成BaSO4 Na2SO3和Na2SO4至少有一种 既有Na2SO3又有Na2SO4
【解析】Ⅰ.A装置中产生的二氧化硫气体中含有水蒸气,水能和过氧化钠反应生成氢氧化钠和氧气,B装置中浓硫酸具有吸水性,可吸收水蒸气;空气中含有二氧化碳和水蒸气,碱石灰是干燥剂,所以能吸收水分,防止水蒸气的干扰,碱石灰能和二氧化碳反应,防止二氧化碳的干扰,所以装置D的作用是防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应C;
Ⅱ.根据题给假设2、假设3可知假设1应该为:只有Na2SO3;(1)若假设2成立,二氧化硫和过氧化钠反应生成硫酸钠,反应的化学方程式为:Na2O2+SO2=Na2SO4。(2)硝酸有强氧化性,加入盐酸后硝酸根离子在酸性条件下能把亚硫酸根离子氧化成硫酸根离子,所以该方案不合理;(3)②滴加过量的1molL-1BaCl2溶液,若产生白色沉淀,由于硫酸钡和亚硫酸钡均为不溶于水的白色固体,则证明C中固体产物中Na2SO3和Na2SO4至少有一种;③滴加适量的1molL-1稀盐酸,若白色沉淀部分溶解,并产生刺激性气味气体,溶解的为亚硫酸钡,不溶的为硫酸钡,则证明C中固体产物中既有Na2SO3又有Na2SO4。


科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是___________。
(2)甲组同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为____________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____。
(4)丙组同学取10 mL 0.1 mol·L-1 KI溶液,加入6 mL 0.1 mol·L-1 FeCl3溶液混合。分别取2 mL 此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是____(填离子符号);实验①和③说明:在I-过量的情况下,
溶液中仍含有___(填离子符号),由此可以证明该氧化还原反应为________。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是_______________;生成沉淀的原因是__________________(用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)9.03×1023个硝酸分子含________mol电子,其中所含氧原子数与_________克CO2中所含氧原子数相等;46g X2O4中含有2.0mol氧原子,则X的摩尔质量为_________
(2)现有下列物质:①氢氧化钠固体 ②稀硫酸 ③铜片 ④蔗糖(C12H22O11)固体 ⑤熔融的氯化钠
用以上物质的序号填空:属于非电解质的是________;所给状态下能够导电的是________
(3)在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应,测得反应前后各物质质量如下表,则该密闭容器中发生的化学反应类型为_____________________
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 5 | 5 | 55 | 5 |
反应后质量/g | 27 | 待测 | 0 | 19 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图利用培养皿探究氨气的性质,实验时向NaOH固体上滴几滴浓氨水,立即用另一培养皿扣在上面。下表中对实验现象的描述及所做的解释均正确的是
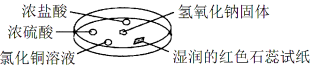
选项 | 实 验 现 象 | 解 释 |
A | 浓盐酸附近产生白烟 | NH3与HCl反应生成了NH4Cl固体 |
B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
C | 氯化铜溶液变白色浑浊 | 白色浑浊的成分是Cu(OH)2 |
D | 湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香叶醇是合成玫瑰香油的主要原料,其结构简式如图:下列有关香叶醇的叙述正确的是( ) 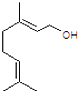
A.香叶醇的分子式为C10H20O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应也能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(NH4)2SO4在一定条件下发生如下反应:4(NH4)2SO4![]() N2↑+6 NH3↑+3SO2↑+SO3↑+7H2O 将反应后的气体通入一定量的BaCl2溶液中,发现溶液有白色沉淀生成,还有部分气体从溶液中逸出,检验发现从溶液中逸出的气体无色、无味,溶液中氯化钡恰好完全反应。下列说法正确的是
N2↑+6 NH3↑+3SO2↑+SO3↑+7H2O 将反应后的气体通入一定量的BaCl2溶液中,发现溶液有白色沉淀生成,还有部分气体从溶液中逸出,检验发现从溶液中逸出的气体无色、无味,溶液中氯化钡恰好完全反应。下列说法正确的是
A.生成沉淀中既有BaSO4、又有BaSO3,且n(BaSO4):n(BaSO3)约为1:1
B.生成沉淀中既有BaSO4、又有BaSO3,且n(BaSO4):n(BaSO3)约为1:2
C.生成沉淀中既有BaSO4、又有BaSO3,且n(BaSO4):n(BaSO3)约为1:3
D.从溶液中逸出的气体只有N2,最后留下溶液中溶质只有较多的NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用下图所示装置制备气体(酒精灯可以根据需要选择),对应说法正确的是

选项 | ①中药品 | ②中药品 | ③中药品 | ④中药品 | 制备气体 | ⑥中药品及作用 |
A | 浓盐酸 | MnO2 | 饱和食盐水 | 浓硫酸 | C12 | NaOH溶液,尾气吸收 |
B | 稀硝酸 | Cu | 烧碱溶液 | 浓硫酸 | NO | Na()H溶液,尾气吸收 |
C | 浓盐酸 | 大理石 | 饱和Na2CO3溶液 | 浓硫酸 | CO2 | 澄清石灰水,检验CO2 |
D | 浓盐酸 | Zn | 水 | 浓硫酸 | H2 | 可撤去 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在298K,1.01×105Pa下,将22g CO2通入750mL 1molL﹣1 NaOH的溶液中充分反应,测得反应放出x kJ的热量.已知在该条件下,1mol CO2通入1L 2molL﹣1 NaOH溶液中充分反应放出y kJ的热量.则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
A.CO2(g)+NaOH(aq)═NaHCO3(aq)△H=﹣(2y﹣x)kJmol﹣1
B.CO2(g)+NaOH(aq)═NaHCO3(aq)△H=﹣(4x﹣y)kJmol﹣1
C.CO2(g)+NaOH(aq)═NaHCO3(aq)△H=﹣(2x﹣y)kJmol﹣1
D.2CO2(g)+2NaOH(l)═2NaHCO3(l)△H=﹣(8x﹣2y)kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com