
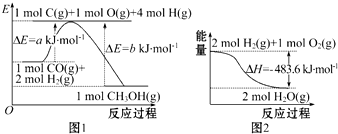
| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者△H小 | |
| C. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
科目:高中化学 来源: 题型:多选题
| A. | 除去BaSO4中的少量BaCO3加入足量盐酸,充分反应后,过滤、洗涤、干燥 | |
| B. | 除去KCl溶液中的少量MgCl2,加入适量NaOH溶液,过滤 | |
| C. | 除去CO2气体中混有的HCl气体:通过饱和碳酸氢钠溶液,洗气 | |
| D. | 除去碘水中的碘,加入乙醇萃取后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Ba2+、NO3-、Cl- | B. | Ca2+、Al3+、Br-、NO3- | ||
| C. | Na+、ClO-、SO42-、HCO3- | D. | Mg2+、Cl-、NH4+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na与O2 | B. | NaOH与CO2 | C. | Na2O与CO2 | D. | Na2O2与H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+ NH4+ SO42-Cl- | B. | Na+Mg2+ HCO3- NO3- | ||
| C. | K+ Na+ AlO2-Cl- | D. | Fe2+ K+NO3-Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14C16O和12C18O两个分子所含质子数、中子数和原子个数均相等 | |
| B. | 1H2和2H2互为同位素,它们的质子数相等 | |
| C. | 14C和14N的质量数相等,它们是同素异形体 | |
| D. | NH4+和H3O+两个离子的电子数、质子数和中子数均相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
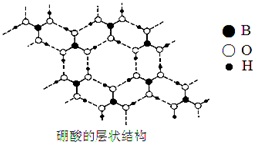 硼(B)及其化合物在化学中有重要的地位.请回答下列问题:
硼(B)及其化合物在化学中有重要的地位.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com