
在一定温度下的定容密闭容器中,以下说法能表明反应:A(s)+2B(g) C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
A.混合气体的压强不变 B.混合气体的密度不变
C.每消耗2molB,同时消耗1molC D.C和D的浓度比不变
科目:高中化学 来源:2014-2015河北省邯郸市高一上学期期末考试化学试卷(解析版) 题型:选择题
在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+的浓度为0.2 mol·L-1,SO42-的浓度为0.6 mol·L-1,则混合溶液中Na+的浓度为
A.0.6 mol·L-1 B.0.15 mol·L-1
C.0.3 mol·L-1 D.0.45 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高一上学期期末考试化学试卷(解析版) 题型:实验题
(10分)某化学兴趣小组进行铁跟水蒸气反应的实验,实验装置如下,发现有黑色晶体生成并产生无色气体,他们继续对反应产物进行探究。
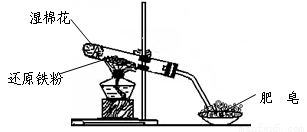
已知:①FeO + 2H+ = Fe2+ + H2O
②Fe2O3 + 6H+ = 2Fe3+ +3 H2O
③Fe3O4 + 8H+ = Fe2+ +2Fe3+ +4 H2O
请回答下列问题:
(1)该组同学欲确定反应一段时间后试管中固体的成分,设计如下实验方案:
①待试管冷却后,取少许其中的固体溶于稀硫酸得溶液B。
②取少量溶液B滴加KSCN溶液,若溶液变红色,则说明试管中固体物质的成分是(只有一个选项符合题意) ,若溶液未变红色,则说明试管中固体物质的成分是(只有一个选项符合题意) 。
A.一定有Fe3O4,可能有Fe
B.只有Fe(OH)3
C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe
E.只有Fe3O4
(2)该组同学取少量溶液B进行了实验,结果②中溶液未变红色,原因是(用离子方程式表示) 。
(3)铁跟水蒸气反应的化学方程为 。
(4)该组同学另取少量溶液B,使其跟NaOH溶液反应。若按下图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出沉淀由白色变成灰绿色最后变成红褐色的反应方程式 。
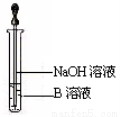
(5)一段时间后,该组同学发现(2)中未变红色的溶液变成红色,说明Fe2+具有 (填化学性质)。由此可知,实验室中含Fe2+的盐溶液需现用现配,并且配制含Fe2+的盐溶液时应加入少量 。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子能大量共存的是
A.K+、Ag+ 、SO42-、Cl- B.H+ 、Na+ 、Cl-、CO32-
C.NH4 + 、Fe3+ 、OH-、Br- D.Na+、NO3.-、OH-、AlO2-
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高二第一学期期末化学试卷(解析版) 题型:填空题
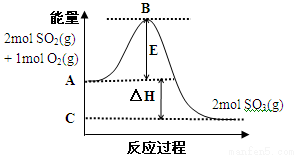
(7分)2SO2(g) + O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99 kJ·mol-1。
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99 kJ·mol-1。
请回答下列问题:
 (1)已知图中C 点表示2mol SO3(g)的总能量,则A点表示: ;E所代表的能量是 ;E的大小对该反应的反应热 影响。(填“有”或“无”)。
(1)已知图中C 点表示2mol SO3(g)的总能量,则A点表示: ;E所代表的能量是 ;E的大小对该反应的反应热 影响。(填“有”或“无”)。
 (2)图中△H= kJ·mol-1。
(2)图中△H= kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高二第一学期期末化学试卷(解析版) 题型:选择题
下列叙述错误的是
A.生铁中含有碳,抗腐蚀能力比纯铁弱
B.铁在潮湿空气中发生腐蚀,其负极反应是2H++2e-=H2↑
C.用锡焊接的铁质器件,焊接处易生锈
D.铁管上镶嵌锌块,铁管不易被腐蚀
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高一上学期期末考试化学试卷(解析版) 题型:填空题
(本小题满分13分)碳酸钠俗称纯碱,在日常生活和生成中有着广泛的应用。某化学兴趣小组想根据所学知识模拟制备碳酸钠,方法如下:先以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3(反应的化学方程式为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl),然后再将NaHCO3制成Na2CO3。

(1)装置乙的作用是 。
为防止污染空气,尾气中含有的 需要进行吸收处理。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有 、 、 。NaHCO3转化为Na2CO3的化学方程式为 。
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品19g完全溶于水制成溶液,然后向此溶液中不断滴加1mol·L-1的稀盐酸直到不再产生气泡,共消耗300ml稀盐酸。请回答下列问题:
根据实验的需要,用11.9mol·L-1的浓盐酸配制1mol·L-1的稀盐酸时,主要用到的玻璃仪器有烧杯、玻璃棒、①量筒、胶头滴管和 (填仪器名称);需要量取的浓盐酸体积为: mL。
②该样品中NaHCO3和Na2CO3的物质的量之比是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高一上学期期末考试化学试卷(解析版) 题型:选择题
分类是化学研究中常用的方法。下列分类方法正确的是
A.根据溶液酸碱性,将化合物分为酸、碱、盐
B.根据分散质微粒直径大小,将分散系分为胶体、浊液和溶液
C.根据水溶液是否导电,将化合物分为电解质和非电解质
D.根据化合物是否来自于有机体,将化合物分为有机物和无机物
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省龙岩市非一级达标校高二上学期期末化学试卷(解析版) 题型:选择题
下列说法错误的是
A.化学反应必然伴随能量的变化
B.放热反应不一定是自发进行
C.化学反应一定有化学键的断裂与形成
D.需要加热才能发生的反应一定是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com