
| A£® | Ź¹¼×»ł³Č±äŗģÉ«µÄČÜŅŗÖŠ£» K+”¢Ba2+”¢AlO2-”¢NO3- | |
| B£® | 1.0mol/LµÄKIČÜŅŗÖŠ£ŗNa+”¢Fe3+”¢Cl-”¢SO42- | |
| C£® | ÓėĀĮ·“Ó¦²śÉś“óĮæĒāĘųµÄČÜŅŗÖŠ£ŗMg2+”¢HCO3-”¢Cl-”¢NO3- | |
| D£® | c£ØH+£©=1”Į10-13mol/LČÜŅŗÖŠ£ŗNa+”¢AlO2-”¢SiO32-”¢PO43- |
·ÖĪö A£®Ź¹¼×»ł³Č±äŗģÉ«µÄČÜŅŗ£¬ĻŌĖįŠŌ£»
B£®Ąė×ÓÖ®¼ä·¢ÉśŃõ»Æ»¹Ō·“Ó¦£»
C£®ÓėĀĮ·“Ó¦²śÉś“óĮæĒāĘųµÄČÜŅŗ£¬ĪŖ·ĒŃõ»ÆŠŌĖį»ņĒæ¼īČÜŅŗ£»
D£®c£ØH+£©=1”Į10-13mol/LČÜŅŗ£¬ĻŌ¼īŠŌ£®
½ā“š ½ā£ŗA£®Ź¹¼×»ł³Č±äŗģÉ«µÄČÜŅŗ£¬ĻŌĖįŠŌ£¬²»ÄÜ“óĮæ“ęŌŚAlO2-£¬¹ŹA“ķĪó£»
B£®Fe3+”¢I-·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬²»Äܹ²“ę£¬¹ŹB“ķĪó£»
C£®ÓėĀĮ·“Ó¦²śÉś“óĮæĒāĘųµÄČÜŅŗ£¬ĪŖ·ĒŃõ»ÆŠŌĖį»ņĒæ¼īČÜŅŗ£¬Ėį¼īČÜŅŗÖŠ¾ł²»ÄÜ“óĮæ“ęŌŚHCO3-£¬¼īČÜŅŗÖŠŅ²²»ÄÜ“óĮæ“ęŌŚMg2+£¬¹ŹC“ķĪó£»
D£®c£ØH+£©=1”Į10-13mol/LČÜŅŗ£¬ĻŌ¼īŠŌ£¬øĆ×éĄė×ÓÖ®¼ä²»·“Ó¦£¬æÉ“óĮæ¹²“ę£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĄė×Ó¹²“ę£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĻ°ĢāÖŠµÄŠÅĻ¢¼°³£¼ūĄė×ÓÖ®¼äµÄ·“Ó¦ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāŃõ»Æ»¹Ō·“Ó¦”¢ø“·Ö½ā·“Ó¦µÄÅŠ¶Ļ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
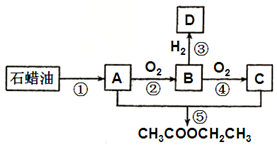 ĢžAŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£®ŅŃÖŖAŌŚ±ź×¼×“æöĻĀµÄĆܶČĪŖ1.25g•L-1£¬BæÉ·¢ÉśŅų¾µ·“Ó¦£®ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼£ŗ
ĢžAŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£®ŅŃÖŖAŌŚ±ź×¼×“æöĻĀµÄĆܶČĪŖ1.25g•L-1£¬BæÉ·¢ÉśŅų¾µ·“Ó¦£®ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2009Äź12ŌĀŌŚøē±¾¹žøłÕŁæŖµÄ¹ś¼ŹĘųŗņ»įŅéŹÜµ½Č«ĒņÕžŅŖµÄ¹ć·ŗ¹Ų×¢£®¼õ»ŗ¹¤ŅµÉś²ś“óĮ涞Ńõ»ÆĮņµÄÅÅ·ÅŅŌŅÖÖĘČ«ĒņĘųŗņ±äÅƳÉĪŖøĆ»įŅéµÄÖ÷Ģā | |
| B£® | Õė¶ŌÄæĒ°¼×ŠĶH1N1Į÷øŠµÄĄ©É¢Ēéæö£¬ŅŖ¼ÓĒæ¶Ō»·¾³”¢øöČĖµÄĻū¶¾Ō¤·Ą£®ĘäÖŠĻū¶¾¼Į³£Ń”ÓĆŗ¬ĀČĻū¶¾¼Į”¢¾Ę¾«”¢Ė«ŃõĖ®µČŹŹŅĖµÄĪļÖŹ | |
| C£® | 2009ÄźÅµ±“¶ūĪļĄķѧ½±ŹŚÓč»ŖŅįæĘѧ¼Ņøßļ棬ŹĒŅņĘäŌŚ¹āĻĖ²ÄĮĻĮģÓņČ”µĆĮĖ×æŌ½¹±Ļ×£®¹āĻĖµÄÖ÷ŅŖ³É·ÖÓėĀźč§ĻąĶ¬£¬Ķس£ĒéæöĻĀ²»ÓėĒæŃõ»Æ¼ĮŗĶĒæĖį·“Ó¦ | |
| D£® | ½Ø¹ś60ÖÜÄźĒģµäĶķ»įÉĻ£¬Ģģ°²ĆÅ¹ć³”Č¼·ÅµÄŃ껚ŹĒijŠ©½šŹōŌŖĖŲ÷ČĮ¦µÄÕ¹ĻÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 28g N2ŗ¬ÓŠµÄŌ×ÓŹżĪŖNA | |
| B£® | 4gCa±ä³ÉCa2+Ź§Č„µÄµē×ÓŹżĪŖ0.1NA | |
| C£® | 1molO2µÄÖŹĮæµČÓŚ1mol OµÄÖŹĮæ | |
| D£® | 24gO2ŗĶ24gO3Ėłŗ¬ÓŠµÄŌ×ÓŹżÄæĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
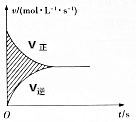 ŌŚČŻ»żĪŖ4LµÄøÕŠŌĆܱÕČŻĘ÷ÖŠ£¬½ųŠŠæÉÄę·“Ó¦£ŗX£Øg£©+2Y£Øg£©?2Z£Øg£©²¢“ļµ½Ę½ŗā£¬ŌŚ“Ė¹ż³ĢÖŠŅŌYµÄÅضČøıä±ķŹ¾µÄ·“Ó¦ĖŁĀŹvÕż”¢vÄęÓėŹ±¼ätµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĶ¼ÖŠŅõÓ°²æ·ÖµÄĆ껿±ķŹ¾£Ø””””£©
ŌŚČŻ»żĪŖ4LµÄøÕŠŌĆܱÕČŻĘ÷ÖŠ£¬½ųŠŠæÉÄę·“Ó¦£ŗX£Øg£©+2Y£Øg£©?2Z£Øg£©²¢“ļµ½Ę½ŗā£¬ŌŚ“Ė¹ż³ĢÖŠŅŌYµÄÅضČøıä±ķŹ¾µÄ·“Ó¦ĖŁĀŹvÕż”¢vÄęÓėŹ±¼ätµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĶ¼ÖŠŅõÓ°²æ·ÖµÄĆ껿±ķŹ¾£Ø””””£©| A£® | XµÄÅØ¶ČµÄ±ä»ÆĮæ | B£® | YµÄÅØ¶ČµÄ¼õŠ”Įæ | ||
| C£® | ZµÄĪļÖŹµÄĮæµÄ±ä»ÆĮæ | D£® | YµÄĪļÖŹµÄĮæµÄ¼õŠ”Įæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
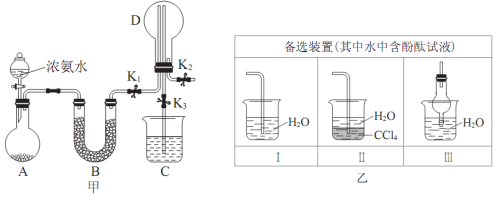
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
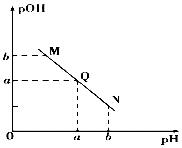 ĻÖÓŠ¢Ł0.1mol/L NaOHČÜŅŗŗĶ¢Ś0.1mol/L HXČÜŅŗ£®
ĻÖÓŠ¢Ł0.1mol/L NaOHČÜŅŗŗĶ¢Ś0.1mol/L HXČÜŅŗ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŽÉ«µÄČÜŅŗÖŠ£ŗFe3+”¢K+”¢NO3-”¢Cl- | |
| B£® | ŗ¬ÓŠ“óĮæBa2+µÄČÜŅŗÖŠ£ŗNH4+”¢Na+”¢Cl-”¢H+ | |
| C£® | pH=13µÄČÜŅŗÖŠ£ŗNH4+”¢Na+”¢SO42-”¢Cl- | |
| D£® | c£ØH+£©=0.1 mol•L-1µÄČÜŅŗÖŠ£ŗK+”¢I-”¢Cl-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠæĮ£ÓėĻ”ĮņĖį·“Ó¦ | B£® | ŃĪĖįÓėĒāŃõ»ÆÄĘ·“Ó¦ | ||
| C£® | Ņŗ»ÆŹÆÓĶĘųµÄČ¼ÉÕ | D£® | ŹÆ»ŅŹÆøßĪĀ·Ö½ā |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com