
【题目】某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如下图。
材料一 NH3是强还原剂,能将某些金属氧化物还原为金属单质或低价态的氧化物。如:2NH3+3CuO ![]() 3Cu+N2+3H2O;
3Cu+N2+3H2O;
材料二 Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu,Cu2O+2H+=Cu2++Cu+H2O。
请回答下列问题:
(1)在实验室里,该学习小组设计下列制取纯净干燥氨气的方案,简易、可行的最佳方案是________。
A.加热氯化铵固体,再通过碱石灰
B.在N2和H2的混合气体中加入铁触媒,并加热至500 ℃,再通过碱石灰
C.加热浓氨水,再通过碱石灰
D.在生石灰中加入浓氨水,再通过碱石灰
(2)为证明NH3还原CuO的反应中有水生成,B中应放入的试剂是。
(3)当观察到(填现象),即表明A中的反应已经完成。
(4)该小组欲用体积比为1∶4的稀硫酸作试剂,检验反应是否有Cu2O固体生成。现用98%的浓硫酸配制1∶4的稀硫酸,所需的玻璃仪器除了胶头滴管外还有。
可证明还原产物中含有Cu2O的操作及现象是。
(5)请写出A中生成Cu2O的化学方程式。
(6)若用定量的方法测定该反应是否生成Cu2O,最简便且准确的方法是。
【答案】
(1)C
(2)无水硫酸铜
(3)A中固体由黑色完全变为红色
(4)烧杯、量筒、玻璃棒;加入硫酸后溶液呈蓝色(其他合理答案也可)
(5)2NH3+6CuO ![]() 3Cu2O+N2+3H2O
3Cu2O+N2+3H2O
(6)称量反应前后装置A中固体的质量
【解析】若加热氯化铵生成的氯化氢气体与氨气继续反应生成氯化铵固体,很难使气体放出,而利用氮气和氢气反应条件太复杂,C、D都可以快速制取氨气,而C用料更简单。反应为通入氨气还原氧化铜,根据固体的颜色变化可以判断反应进行的程度。根据Cu+在酸性溶液中的不稳定性来判断。
【考点精析】解答此题的关键在于理解氨的化学性质的相关知识,掌握与水反应,NH3是惟一能使润湿的红色石蕊试纸交蓝的气体,常用此性质检验NH3;与酸反应:NH3+HCl=NH4Cl(生成白烟);与O2反应:4NH3+5O2=4NO+6H2O+Q;


科目:高中化学 来源: 题型:
【题目】下列鉴别方法不合理的是
A. 用溴水鉴别苯和己烯 B. 用银氨溶液鉴别甲酸和乙醛
C. 用金属钠鉴别乙醇和乙醚 D. 用碳酸钠溶液鉴别乙酸和乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(气)+3H2(气)![]() 2NH3(气) ΔH<0,下列说法正确的是( )
2NH3(气) ΔH<0,下列说法正确的是( )
A.达到平衡时反应物和生成物浓度一定相等
B.达到平衡后加入氨气,重新达到平衡时,氨气的浓度比原平衡时大
C.达到平衡时,升高温度加快了吸热反应的速率,降低了放热反应的速率,所以平衡向逆反应的方向移动
D.加入催化剂可以缩短到达平衡的时间,这是因为加快了正反应的速率,而减慢了逆反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. NH4+的检验:加入氢氧化钠溶液,加热,用湿润的蓝色石蕊试纸在试管口检验
B. 工业合成氨的反应中,如果氮气过量,氢气能完全反应
C. 石灰石与稀硫酸不能持续产生二氧化碳
D. 形成喷泉的原因一定是内部的压强大于外界大气压
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示的装置是仿照工业制备硫酸的工艺流程设计出来的,用于探究工业上为何采用98.3%的浓硫酸吸收三氧化硫。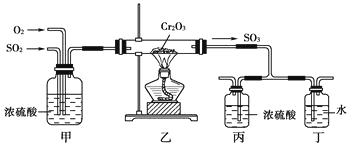
试填写下列空白:
(1)写出工业上用FeS2制取SO2的化学方程式:。
(2)写出上图中部分装置的作用:①甲;
②丙和丁:。
(3)若丁装置在反应过程中出现气泡,不久就出现了白雾,而丙装置一直没有明显变化,产生这种现象的可能原因是:①丙中插入浓硫酸中的导管插入太深,使两个吸收瓶内的压强差较大,导致SO3从丁的水中冒了出来,与水形成酸雾:②。
(4)上图装置中的甲和乙部分、丙和丁部分分别与工业制取硫酸的装置相对应,甲和乙相当于;丙和丁相当于。
(5)在硫酸工业制法中,下列对生产操作与说明生产操作的主要原因的叙述都正确的是________(填下列选项的序号)。
A.硫铁矿燃烧前需要粉碎,因为大块的硫铁矿不能在空气中燃烧
B.从沸腾炉出来的炉气需净化,因为炉气中二氧化碳会与杂质反应
C.二氧化硫氧化为三氧化硫时需使用催化剂,这样可以提高二氧化硫的转化率
D.三氧化硫用98.3%的浓硫酸溶液吸收,目的是防止形成酸雾,以提高三氧化硫的吸收效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用氟磷灰石[Ca5(PO4)3F]为原料,按如下图所示流程制取磷酸、重过磷酸钙[Ca(H2PO4)2]和氢氟酸。图中反应(Ⅰ)为氟磷灰石跟另一种原料反应,生成A、B、C三种物质,其中的产物C又跟氟磷灰石发生反应(Ⅱ),生成B和重过磷酸钙。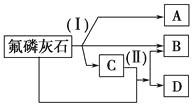
试写出两个反应的化学方程式:反应(Ⅰ);反应(Ⅱ)。
在生产中要特别注意
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中于一定条件下进行下列反应:2SO2+O22SO3当到达平衡时通入18O2 , 再次平衡时,18O存在于( )
A.SO2、O2
B.SO2、SO3
C.O2、SO3
D.SO2、O2、SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com