
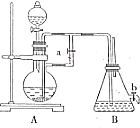
 如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的须色变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.
如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的须色变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.分析 (1)A中应预先盛放固态反应物,铁和稀硫酸发生氧化还原反应生成硫酸亚铁和氢气;
(2)实验开始时,应先打开活塞,使生成的氢气充满整套实验装置中而排出空气,防止氢氧化亚铁被氧化;
(3)关闭活塞时,在气体压强的作用下,A中溶液进入B装置中,A中溶液含有硫酸亚铁,可能含有硫酸,硫酸和硫酸亚铁都和氢氧化钠溶液反应,硫酸亚铁和氢氧化钠溶液反应生成氢氧化亚铁;
(4)氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀.
解答 解:(1)A中应预先盛放固态反应物铁屑,铁和稀硫酸反应生成硫酸亚铁和氢气,离子反应方程式为:Fe+2H+=Fe2++H2↑,
故答案为:铁屑;Fe+2H+=Fe2++H2↑;
(2)实验开始时,应先打开活塞,使生成的氢气进入整套实验装置中而排出空气,防止氢氧化亚铁被氧化,
故答案为:打开;
(3)A中反应发生后,为保证硫酸亚铁进入B中和氢氧化钠混合,要借助氢气产生的压强,所以需要关闭活塞a,在气体压强的作用下,A中含有硫酸亚铁溶液被压人B中,硫酸亚铁和氢氧化钠溶液反应,发生的离子反应方程式为:Fe2++2OH-=Fe(OH)2↓,生成Fe(OH)2白色沉淀,
故答案为:关闭活塞a,在气体压强的作用下,A中含有硫酸亚铁溶液被压人B中,硫酸亚铁和氢氧化钠溶液反应;
(4)氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀,所以实验完毕,打开b处活塞,放入一部分空气,出现白色沉淀先转化为灰绿色最后转化为红褐色,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查了氢氧化亚铁的制取,题目难度中等,氢氧化亚铁易被氧气氧化,所以制取氢氧化亚铁时注意必须在无氧气条件下进行反应,这是高中化学中较重要的一个实验,是学习重点.注意正确书写反应方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2溶液与少量Ca(OH)2溶液反应:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| B. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═2HClO+SO32- | |
| C. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
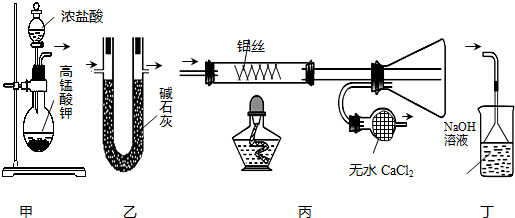
| A. | 用装置甲制取氯气 | B. | 用装置乙干燥氯气 | ||
| C. | 用装置丙制取并收集AlCl3 | D. | 用装置丁处理丙中排出的尾气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
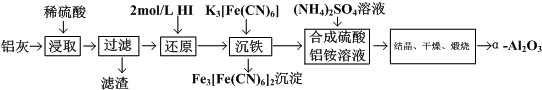
| A. | 加热搅拌可以提高铝灰的浸取率 | |
| B. | 流程中的HI,可以用H2O2代替 | |
| C. | 流程中的K3[Fe(CN)6],可以用NaOH溶液代替 | |
| D. | 流程中的得到硫酸铝按晶体的具体方法为:蒸发结晶、趁热过滤、洗涤、干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸发、冷却结晶和过滤的方法从氯化钠和硝酸钾的混合溶液中离出硝酸钾 | |
| B. | 用分液的方法分离乙酸乙酯的饱和碳酸钠溶液 | |
| C. | 用加热的方法提纯含有少量碳酸氢钠的碳酸钠 | |
| D. | 用加水溶解、过滤的方法提含有硫酸钠的碳酸钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
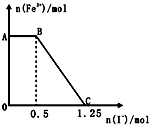 已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应的方程式为:2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的 物质的量的变化关系如图所示,则下列有关说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应的方程式为:2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的 物质的量的变化关系如图所示,则下列有关说法不正确的是( )| A. | 图中AB段主要是高锰酸钾和碘化钾溶液反应 | |
| B. | 图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 | |
| C. | 根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol | |
| D. | 向C点以后的溶液中加入少量KSCN溶液,溶液变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4和NaOH反应的中和热是HCl和NaOH反应的中和热的两倍 | |
| B. | CO的标准燃烧热是△H=-283.0KJ/mol,则反应2CO2(g)═2CO(g)+O2(g)的△H=+566.0KJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 甲烷完全燃烧生成液态水和二氧化碳气体所放出的热量是甲烷的标准燃烧热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com