
| 溶解 |
| ① |
| BaCI2 |
| ② |
| NaOH |
| ③ |
| NaCO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5mL水 |
| B、10 mL 0.2 mol?L-1 MgCl2溶液 |
| C、20 mL 0.5 mol?L-1 NaCl溶液 |
| D、40mL 0.1 mo1?L-1盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| |温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
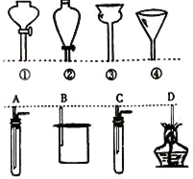 ①②③④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图(仪器中的药品及铁架台、铁夹等其它物品均已略去).请根据实际使用操作时上述漏斗的适用范围和它们的形状,指出A、B、C、D分别与①②③④中哪一种或哪几种最为匹配.A与
①②③④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图(仪器中的药品及铁架台、铁夹等其它物品均已略去).请根据实际使用操作时上述漏斗的适用范围和它们的形状,指出A、B、C、D分别与①②③④中哪一种或哪几种最为匹配.A与查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在晶体中只要有阳离子就一定有阴离子 |
| B、加热至沸腾蒸发水分时,溶液的浓度一定增大 |
| C、一个原子或单核离子,最外层有8个电子时,一定达到了稳定结构 |
| D、水的分子量不到空气平均分子量的2/3,如果水分子间没有特殊的作用力,地球上就不会有液态水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com