
| A. | KBr | B. | NaOH | C. | HBr | D. | Na2O2 |
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铝粉和MnO2制得锰 | |
| B. | 用电解熔融氯化铝的方法制得单质铝 | |
| C. | 氯化铝溶液和过量氢氧化钠溶液反应制备Al(OH)3 | |
| D. | 用镁粉和空气反应制备Mg3N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
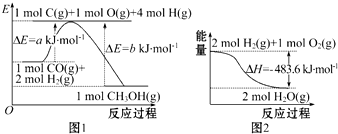
| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者△H小 | |
| C. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯、四氯化碳用溴水即可鉴别 | |
| B. | CH3CH2OH、CH3COOH均可与金属Na反应生成H2 | |
| C. | 糖类、蛋白质、油脂都能发生水解反应 | |
| D. | 等物质的量的乙烯、乙醇分别完全燃烧,消耗O2的质量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2,3-二甲基-丁烷
2,3-二甲基-丁烷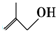 的分子式为C4H8O;
的分子式为C4H8O;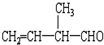 官能团的名称是碳碳双键、醛基.
官能团的名称是碳碳双键、醛基.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com