
【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其化学平衡常数为K2,在温度973K和1173K的情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其化学平衡常数为K2,在温度973K和1173K的情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973K | 1.47 | 2.38 |
1173K | 2.15 | 1.67 |
请填空:
(1)反应①的K1表达式是___。
(2)现有反应③:CO2(g)+H2(g)![]() CO(g)+H2O(g),该反应的平衡常数K3,根据反应①与②可推导出K1、K2与K3之间的关系式为__,据此关系式及上表数据,能推断出反应③是__(填“吸热”或“放热”)反应。
CO(g)+H2O(g),该反应的平衡常数K3,根据反应①与②可推导出K1、K2与K3之间的关系式为__,据此关系式及上表数据,能推断出反应③是__(填“吸热”或“放热”)反应。
(3)能判断反应③一定处于化学平衡状态的依据是___(填写字母序号)。
A.压强不随时间改变
B.气体密度不随时间改变
C.H2的体积分数不随时间改变
D.单位时间内生成H2和H2O(g)的物质的量相等
(4)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:
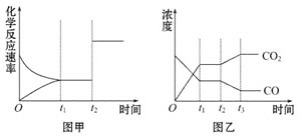
①图甲中t2时刻发生改变的条件是___。
②图乙中t2时刻发生改变的条件是__。
(5)一定条件下处于化学平衡状态的反应③当使CO2和CO的浓度同时增大为原来的两倍时,该反应的化学平衡向__移动(填“不”、“逆反应方向”或“正反应方向”)
【答案】![]()
![]() 吸热 CD 增大压强或使用催化剂 降低温度 不
吸热 CD 增大压强或使用催化剂 降低温度 不
【解析】
⑴反应①得出平衡常数。
⑵方程式相减,平衡常数相除;由表格数据可知,当温度升高时,K1增大,K2减小,故温度升高时,K 3增大,说明温度升高,平衡正向移动,因此正反应为吸热反应。
⑶A. 该反应在反应前后气体分子数不变,因此反应过程中压强一直不变,则压强不随时间变化,不能说明正逆反应速率相等,因此不能判断处于平衡状态;B. 该反应中反应物和生成物都是气体,根据质量守恒定律可得,反应过程中混合气体的质量保持不变,由于反应前后气体分子数不变,因此反应过程中混合气体的体积不变,故反应过程中,混合气体的密度一直不变,则密度不变,不能体现正逆反应速率相等,因此不能判断反应处于平衡状态;C. 反应过程中,H2的体积分数发生变化,当其不变时,说明反应达到平衡状态;D. 生成H2为逆反应,生成H2O(g)为正反应,若单位时间内生成H2和H2O(g)的物质的量相等,说明正逆反应速率相等,反应达到平衡状态。
⑷①图甲t2时,正逆反应速率同等程度增大,平衡不移动,则改变的条件为加入催化剂;由于反应③在反应前后气体分子数不变,因此增大压强,平衡不移动;②图乙t2时,c(CO2)增大,c(CO)减小,平衡逆向移动,由于该反应为吸热反应,因此改变的条件为降低温度。
⑸反应③为气体分子数不变的反应,因此同时增大CO2和CO的浓度为原来的两倍时,化学平衡不移动。
⑴反应①的平衡常数![]() ;
;
⑵反应③的平衡常数![]() ,反应②的化学平衡常数
,反应②的化学平衡常数![]() ,因此反应③的平衡常数
,因此反应③的平衡常数![]() ;由表格数据可知,当温度升高时,K1增大,K 2减小,故温度升高时,K 3增大,说明温度升高,平衡正向移动,因此正反应为吸热反应;故答案为:
;由表格数据可知,当温度升高时,K1增大,K 2减小,故温度升高时,K 3增大,说明温度升高,平衡正向移动,因此正反应为吸热反应;故答案为:![]() ;吸热。
;吸热。
⑶A. 该反应在反应前后气体分子数不变,因此反应过程中压强一直不变,则压强不随时间变化,不能说明正逆反应速率相等,因此不能判断处于平衡状态,故A不符合题意;B. 该反应中反应物和生成物都是气体,根据质量守恒定律可得,反应过程中混合气体的质量保持不变,由于反应前后气体分子数不变,因此反应过程中混合气体的体积不变,故反应过程中,混合气体的密度一直不变,则密度不变,不能体现正逆反应速率相等,因此不能判断反应处于平衡状态,故B不符合题意;C. 反应过程中,H2的体积分数发生变化,当其不变时,说明反应达到平衡状态,故C符合题意;D. 生成H2为逆反应,生成H2O(g)为正反应,若单位时间内生成H2和H2O(g)的物质的量相等,说明正逆反应速率相等,反应达到平衡状态,故D符合题意;综上所述,答案为CD。
⑷①图甲t2时,正逆反应速率同等程度增大,平衡不移动,则改变的条件为加入催化剂;由于反应③在反应前后气体分子数不变,因此增大压强,平衡不移动;故t2时刻改变的条件为增大压强或加入催化剂;故答案为:增大压强或使用催化剂。
②图乙t2时,c(CO2)增大,c(CO)减小,平衡逆向移动,由于该反应为吸热反应,因此改变的条件为降低温度;故答案为:降低温度。
⑸反应③为气体分子数不变的反应,因此同时增大CO2和CO的浓度为原来的两倍时,化学平衡不移动;故答案为:不。


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
【题目】在100℃时,把0.5molN2O4通入体积为5L的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L-1。在60s时,体系已达平衡,此时容器内压强为开始时的1.6 倍。下列说法正确的是
A.前2s以N2O4的浓度变化表示的平均反应速率为0.01mol·L-1·s-1
B.在2s时体系内的压强为开始时的1.1倍
C.在平衡时体系内N2O4的物质的量为0.25mol
D.平衡时,N2O4的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,把SiO2细粉放入蒸馏水中,搅拌至平衡,生成H4SiO4溶液(SiO2+2H2OH4SiO4),该反应平衡常数K随温度的变化如图示,搅拌1小时,测得H4SiO4的质量分数为0.01%(溶液密度为1.0g/mL),下列分析正确的是( )
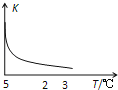
A.该反应平衡常数的表达式为K=c(H4SiO4)
B.该生成H4SiO4的反应为吸热反应
C.用H4SiO4表示的反应速率为1.04×10﹣2mol/(Lh)
D.若K值变大,在平衡移动时逆反应速率先减小后增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的是可逆反应A+2B![]() 2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
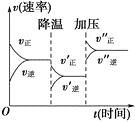
A.该反应的正反应是吸热反应
B.若A,B是气体,则D一定是纯液体或固体
C.该反应的平衡常数始终没变
D.A的转化率最终增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢是应用广泛的“绿色”氧化剂,酸性条件下稳定,中性或弱碱性条件下易分解.填空:
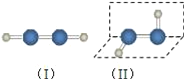
(1)过氧化氢的分子结构如图(Ⅱ),则过氧化氢属于__(极性/非极性)分子.过去曾经有人认为过氧化氢的分子结构也可能是(Ⅰ),选择合理实验方法证明过氧化氢的分子结构为(Ⅱ)__(选填编号).
a.测定过氧化氢的沸点
b.测定过氧化氢分解时的吸收的能量
c.测定过氧化氢中H﹣O和O﹣O的键长
d.观察过氧化氢细流是否在电场中偏转
Na2O2,K2O2以及BaO2都可与酸作用生成过氧化氢.实验室可用稀硫酸和过氧化物在用冰冷却的条件下反应制取过氧化氢.
(2)上述过氧化物中最适合的是__,反应完毕后__(填操作名称)即可得到双氧水.
(3)若反应时没有用冰冷却,会有气体产生,写出反应的化学方程式__.用酸性高锰酸钾溶液滴定双氧水的方法可以测定双氧水的浓度.
(4)取5.00mL 双氧水样品,配制成250mL溶液.此实验过程必须用到的两种主要仪器为__(填仪器名称).
(5)取25.00mL上述溶液,用0.020mol/L的酸性高锰酸钾溶液滴定,看到__,到达滴定终点,消耗高锰酸钾溶液15.50mL.则原双氧水样品中含过氧化氢__ g/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空
(1)打火机、运动会中的火炬一般采用丙烷(C3H8)为燃料。丙烷热值较高,污染较小,是一种优良的燃料。已知一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化如图,请写出表示丙烷燃烧热的热化学方程式:__。
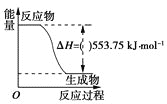
(2)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
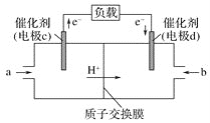
①电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是__(填“正极”或“负极”),c电极的反应方程式为___。
②用该燃料电池电解1L饱和食盐水(足量),当燃料电池消耗0.56L(标准状况下)氧气时,溶液pH=___(不考虑溶液体积变化)。
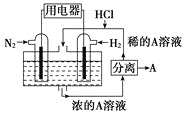
(3)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是__,该反应能设计成原电池的原因是__。A是__(填物质名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学常用的酸碱指示剂酚酞的结构简式如图所示,下列关于酚酞的说法错误的是( )
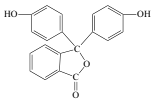
A.酚酞的分子式为C20H14O4
B.酚酞具有弱酸性,且属于芳香族化合物
C.1mol酚酞最多与2molNaOH发生反应
D.酚酞在碱性条件下能够发生水解反应,呈现红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500mL2mol/LNaOH溶液完全吸收,生成NaNO3和NaNO2的混合溶液,其中生成的NaNO3的物质的量为( )
已知NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH= NaNO3+NaNO2+H2O,
A. 0.2mol B. 0.4mol C. 0.6mol D. 0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。某工厂以孔雀石为主要原料制备CuSO4·5H2O,主要步骤如下:
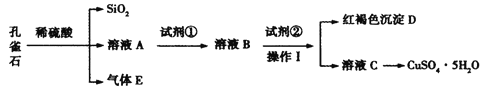
已知该条件下,通过调节溶液的酸碱性而使 Fe3+、Fe2+、Cu2+生成沉淀的 pH 分别如下:
物质 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe(OH)3 | 2.2 | 3.2 |
Fe(OH)2 | 7.6 | 9.6 |
Cu(OH)2 | 4.7 | 6.4 |
请回答下列问题:
(1)为了提高孔雀石酸浸时的速率,除适当增加浓硫酸浓度外,还可以采取的措施有:___(写一种)。
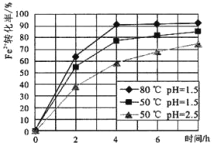
(2)试剂①是双氧水,把 Fe2+氧化成 Fe3+的目的是___。根据如图有关数据,你认为工业上氧化操作时应采取的条件是___。
(3)试剂②为CuO,其目的是调节溶液的 pH 保持在___范围。操作Ⅰ的名称是___。
(4)溶液 C 得到CuSO4·5H2O的主要步骤是___、___、过滤、洗涤、干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com